脂质纳米颗粒(LNPs)在新冠疫情期间证明了其价值,成为核酸类疗法中耐受性良好且高效的载体。LNPs制造更为简便,无需生产细胞系,并可采用标准的体外转录(IVT)mRNA生产流程来制作不同的表达盒。在这一突破基础上,研究人员现正将LNPs应用于体内基因组编辑与调控,有望治疗罕见和常见疾病。正在进行的临床试验在多种应用方面显示出令人鼓舞的结果。
以下章节将重点介绍LNPs的工作原理,以及它们如何推动新的基因疗法从实验室走向临床。
目录
基因治疗与高效递送的需求体内递送
要理解为何递送是如此关键的挑战,首先需要了解现代基因编辑系统在分子层面上是如何工作的。
Cas9-sgRNA复合物在基因组编辑中的机制
目前研究最为透彻的基因组编辑系统是CRISPR-Cas9。其核心工作流程包括三个步骤:识别、切割和修复。该系统将Cas9核酸酶与单导向RNA(sgRNA)配对,sgRNA像分子GPS一样引导Cas9/gRNA复合物定位到匹配的DNA序列。在找到一个短识别基序(PAM,即SpCas9为5′-NGG-3′)后,Cas9解旋DNA并造成双链断裂。随后,细胞通过两种途径之一修复这一断裂:
- 非同源末端连接(NHEJ):引入小的插入或缺失,可能导致基因功能丧失
- 同源重组修复(HDR):在提供供体DNA模板时,实现精确的编辑或插入
这种巧妙的系统使得选择性地破坏、修正或插入基因序列成为可能,并且具有极高的精确性。
脂质纳米颗粒(LNP)用于体内基因组编辑
为了将概念转化为治疗,CRISPR组件——通常是核酸酶mRNA和sgRNA——必须在给药后被递送到细胞内部。脂质纳米颗粒(LNP)通过包裹RNA载荷,在循环中保护其稳定,并确保其被靶向组织高效吸收,从而实现这一目标。一旦递送到位,该系统即可定向修复致病基因,为多种疾病带来“一次治愈”的治疗可能。
LNPs的结构及优势
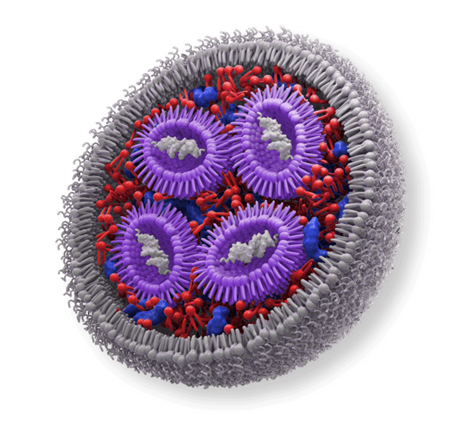
LNP是一种纳米级载体,直径通常约为50-200纳米,可自组装包裹RNA货物。其各组成部分协同工作:
- 可离子化脂质包装RNA并促进其释放到细胞内。
- 辅助磷脂和胆固醇稳定结构并有助于膜融合。
- PEG-脂质体(PEG-lipids)延长循环时间,防止颗粒聚集,并有助于确保颗粒大小均一。
LNPs是可适应的递送载体。与需要生产者细胞系的病毒颗粒不同,它们完全是合成且可扩展的。同一种LNP配方可以包裹不同的mRNA设计,这些设计可以通过基因合成和IVT生产迅速优化。LNPs能够携带不同格式的CRISPR(mRNA、sgRNA或核糖核蛋白复合物),其组成还可以通过靶向配体进行修饰,实现细胞特异性递送。它们表现出低免疫原性,并在需要时支持重复给药。这些能力使LNPs成为推动基因组编辑疗法走向临床现实的核心技术。
脂质化学和配方方面的最新进展,正在进一步拓展递送范围,不仅限于肝脏
——通常是系统给药后LNP积累的主要部位——还包括其他类型细胞,如免疫细胞以及骨髓中的造血干细胞(HSCs)。
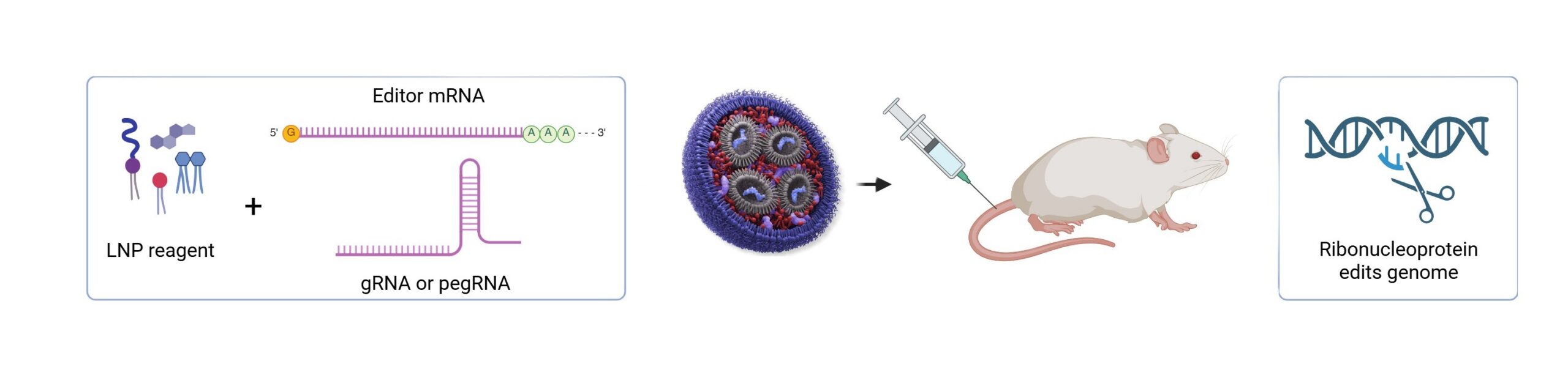
图1. 体内基因组编辑流程。编辑酶mRNA和gRNA被包裹在LNP中,体内递送后,被翻译为核糖核蛋白复合物,在基因组中引入定点编辑(见示意图,上图)。
关键LNP赋能的基因编辑技术
- Cas9介导的编辑– Cas9核酸酶在DNA中产生双链断裂(DSB)。通过易出错的非同源末端连接(NHEJ)可实现基因敲除,而精确修复则需要供体DNA和同源重组修复(HDR)。LNP通常以mRNA形式递送编辑器,且mRNA半衰期较短,有助于防止脱靶编辑。
然而,传统的Cas9编辑仍存在通过双链断裂(DSB)导致染色体重排和脱靶效应的风险。为了解决这些问题,研究人员开发了Cas9切口酶,它只切割一条DNA链,为下一代编辑工具奠定了基础。
- 碱基编辑– 通过将Cas9切口酶与脱氨酶融合,碱基编辑器能够直接实现A→G或C→T的转换,无需引入DSBs,从而纠正疾病相关SNP或通过破坏外显子剪接或引入终止密码子来敲除基因。虽然高度精准,但目前仅限于这两种碱基替换,并可能导致附近“旁观者”位点的非预期编辑。
- 引物编辑(Prime Editing)– 最新进展是引物编辑,它结合了Cas9切口酶和逆转录酶,可以实现小片段插入、缺失以及全部12种可能的碱基间转换——无需供体DNA模板,也不会产生DSBs。引物编辑拓宽了可治疗突变的范围,并已进入临床阶段,如Prime Medicine公司针对慢性肉芽肿病开展的PM359临床试验。目前,该研究正在使用引物编辑进行对离体造血干细胞的调控,但随着该技术日益成熟,可预见未来将应用于体内递送。
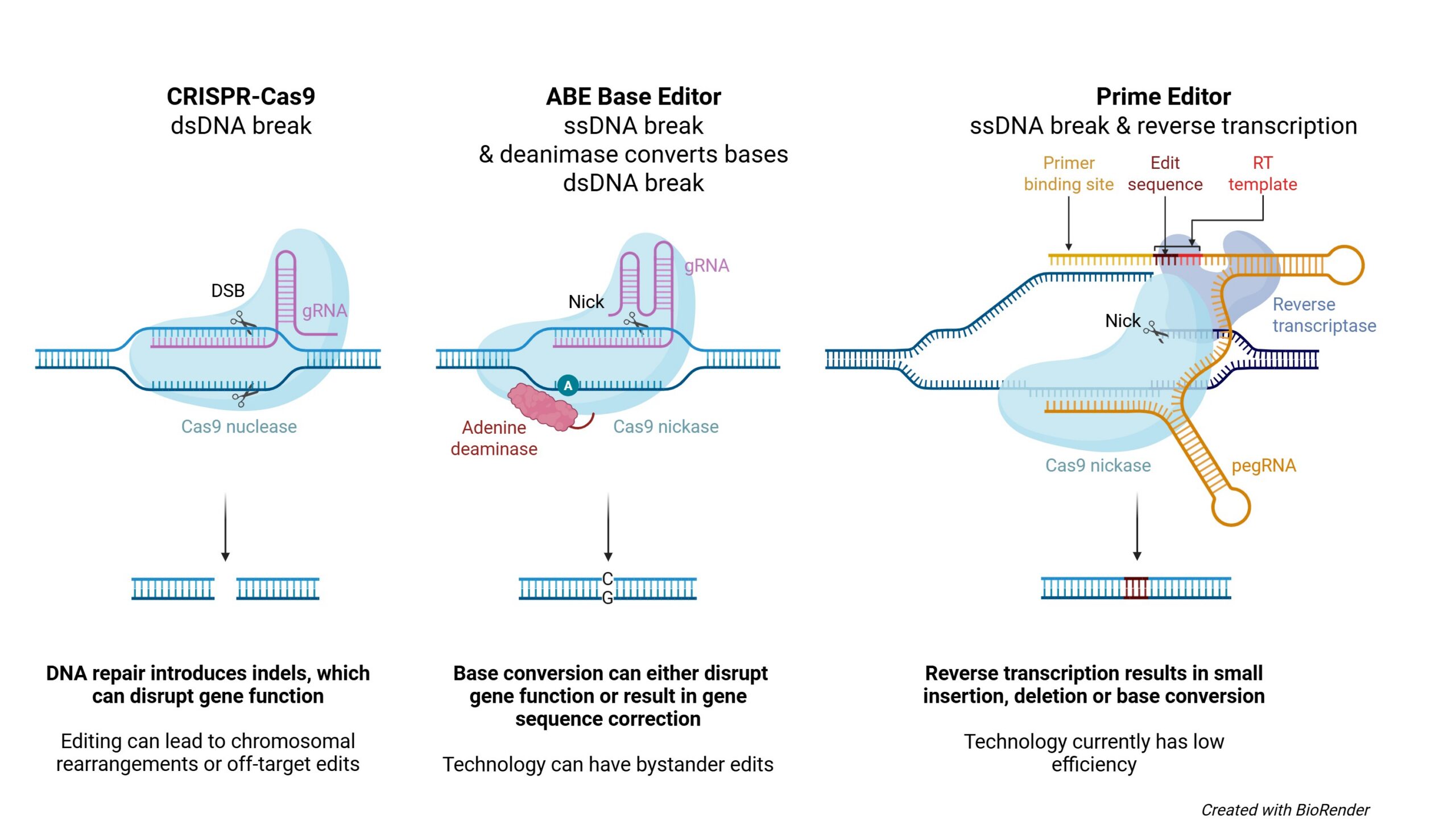
图2. 不同基因编辑技术的机制。Cas9 通过产生DNA双链断裂并由DNA修复通路修复(左图)。碱基编辑器通过脱氨酶活性实现靶向核苷酸替换(见中间图)。引导编辑器无需造成双链断裂,直接将新的遗传信息“写入”DNA(右图)。
新兴的临床应用体内脂质纳米颗粒递送的基因编辑
不断增长的临床和前临床数据强调了其变革性的潜力,用于基因编辑的脂质纳米颗粒,在广泛的治疗领域中。
- 罕见遗传病的持久治疗– 首批利用LNP技术实现的体内CRISPR-Cas9基因组编辑的临床研究由Intellia Therapeutics公司率先开展,重点针对两种罕见疾病:遗传性血管性水肿(HAE)和ATTR淀粉样变性。HAE是一种罕见且可能危及生命的疾病,其特征为反复发作的肿胀,可导致气道阻塞并严重影响生活质量。同样,ATTR淀粉样变性是一种进行性疾病,由错误折叠的转甲状腺素蛋白沉积引起,损害神经和器官,导致神经病变、心肌病和早逝。Intellia目前正在对这些疾病进行三期临床试验。Intellia Therapeutics已经证明,体内CRISPR编辑能够在这两种疾病中产生持久疗效,一次性输注即可实现高效且持久的治疗效果,并可持续至少2-3年。
- 常见疾病风险因素的预防–Verve Therapeutics(最近被礼来公司收购)是首个将基因组编辑应用于常见疾病,而非罕见疾病的团队——他们针对的是家族性高胆固醇血症(FH),这种疾病影响着全球每300人中的1人。体内FH是一种遗传性疾病,与升高的低密度脂蛋白胆固醇有关,会导致受影响人群过早发生心血管疾病。目前的治疗方法——包括他汀类药物和PCSK9抑制剂——往往效果有限,因此亟需持久、长期有效的治疗方案。Verve Therapeutics正在开发Verve-102,一种体内基因碱基编辑疗法,通过GalNAc-LNP递送系统靶向肝脏中的PCSK9基因。在早期临床试验中,单次注射Verve-102耐受性良好,并显著且持续地降低了低密度脂蛋白胆固醇。如果在更大规模研究中得到证实,这些项目有望将动脉粥样硬化性心血管疾病的治疗方式从每日反复服药转变为一次给药,终身受益.
- 针对极罕见儿科疾病的快速个性化治疗——2025年5月,来自美国国立卫生研究院(NIH)和费城儿童医院的研究人员报道了首例个性化治疗方案体内基因碱基编辑疗法,用于一名7个月大的患有极罕见遗传病(氨基甲酰磷酸合成酶I(CPS1)缺乏症)的婴儿. CPS缺乏症是一种极为罕见的尿素循环障碍,会在出生后不久导致有毒氨的积聚,引发严重的神经损伤和死亡。目前尚无治愈性疗法。该治疗方案在诊断后数月内被设计、制造并实施,早期结果显示能够安全纠正代谢缺陷。此项治疗展现了基于LNP的基因组编辑疗法的卓越速度和模块化特性。本案例强调了快速适应性平台如何能够将治愈性疗法扩展至最罕见且时间最为紧迫的遗传疾病.
为基因治疗应用选择合适的脂质纳米颗粒
选择合适的脂质纳米颗粒对于基因治疗的成功至关重要。并非所有LNP都同样适用于治疗用途,推进LNP进入临床时,必须仔细评估多项因素,包括将基因组编辑载荷递送到正确细胞的效力、耐受性、可扩展性/稳定性,以及在相关动物模型中的验证。体内脂质纳米颗粒正迅速成为体内基因组编辑首选递送载体,其应用范围涵盖从罕见病治疗到心血管疾病。最新临床与前临床数据证明了其用于治疗时的效力、持久性和可扩展性:
基因递送用LNPs的关键要点
脂质纳米颗粒正迅速成为体内基因编辑的首选递送载体,应用范围涵盖从罕见疾病治疗到心血管疾病。最新的临床和前临床数据展示了它们在治疗中的高效性、持久性和可扩展性。
- 经临床验证的疗效:LNPs在新冠疫情期间得到了广泛应用,如今正在推动体内基因组编辑在多种疾病领域的发展。
- 持久的一次性疗法:单剂量治疗可带来多年益处
- 广泛的治疗覆盖面:基于LNP的编辑项目正在推进,用于治疗罕见疾病以及高胆固醇等常见病症。
- 快速个性化:NIH CPS1婴儿案例展示了LNP平台的模块化和快速响应能力,即使在极其罕见的情况下也是如此。
关键选择因素:在选择具有开发治疗潜力的LNP时,效力、大型动物(包括非人灵长类动物)中的验证、高剂量耐受性以及可扩展性/稳定性都是至关重要的。
关于脂质纳米颗粒和基因组编辑的更多资源
对于有兴趣深入了解的读者,赛默飞世尔科技为开发基于脂质纳米颗粒递送系统进行基因编辑的研究人员提供了一系列工具、产品和教育资源:
仅供科研使用。不得用于诊断程序。
© 2026 赛默飞世尔科技公司版权所有。除非另有说明,所有商标均为赛默飞世尔科技及其子公司的财产。
参考文献
- https://www.nih.gov/news-events/news-releases/infant-rare-incurable-disease-first-successfully-receive-personalized-gene-therapy-treatment
- https://www.fiercebiotech.com/biotech/crispr-therapeutics-sees-80-fall-ldl-triglycerides-after-vivo-liver-editing
- https://ir.vervetx.com/news-releases/news-release-details/verve-therapeutics-announces-positive-initial-data-heart-2-phase
- Intellia Announces Positive Two-Year Follow-Up Data from Ongoing Phase 1 Study of Nexiguran Ziclumeran (nex-z), in Patients with Hereditary Transthyretin (ATTR) Amyloidosis with Polyneuropathy at Peripheral Nerve Society Annual Meeting – Intellia Therapeutics
- Intellia Therapeutics Announces Positive Three-Year Data
- https://investors.primemedicine.com/news-releases/news-release-details/prime-medicine-presents-vivo-proof-concept-data-highlighting

发表回复