癌症类器官是从患者肿瘤样本中获得的三维细胞培养物。癌症类器官模型(也称为肿瘤类器官模型)能够准确模拟实际肿瘤的突变特征、基因表达水平和物理结构,为癌症研究提供了宝贵工具。然而,这种更高的生物相关性也带来了与二维(2D)细胞系相比,在监测和处理肿瘤类器官方面的一些差异,并且它们在三维(3D)培养过程中会表现出多种不同的形态。
OncoPro 肿瘤类器官培养基旨在支持来自多种癌症类型的肿瘤类器官生长,采用易于配制的培养基,兼容基底膜提取物(BME)水凝胶中的嵌入式培养以及悬浮培养在非组织培养处理的培养皿和瓶中。使用标准化的肿瘤类器官培养基可以消除细胞培养流程中的变异性,并且最好与专门针对肿瘤类器官制定的细胞培养方案搭配使用。本博客文章为您提供实用建议,帮助您应对癌症类器官培养过程中的复杂性,让具有生理相关性的、来源于患者的癌症细胞培养比以往更加便捷可及。
3D 癌症类器官的形态学特征
肿瘤类器官形态可能因供体而异,即使是在同一种类型的癌症中。这种差异强调了在癌症研究和治疗中采用个性化方法的重要性,以及利用反映临床癌症病例广泛异质性的患者来源肿瘤类器官面板的重要性。每一个类器官模型都可能呈现出依赖于供体的生长模式和结构特征。其形态可以从囊状结构
——即一层薄薄的细胞包围着充满液体的中心——到更为坚实或葡萄状结构不等。下方展示了不同时间点肿瘤类器官代表性图像,以说明其变化过程类器官细胞在最初接种单个细胞和小型细胞团后,会组装成供体依赖性的三维结构,并随着时间推移而增大。在培养过程中,必须进行仔细监测,我们建议通过显微镜频繁检查类器官。当类器官直径达到约100-300微米时即可进行传代,对于大多数培养物,这通常发生在接种后6-10天,但也可能在培养5-14天后出现。过度生长会导致类器官核心坏死,在明场显微镜下表现为暗色且致密的区域。过度坏死可能导致培养失败,因此当类器官直径达到约100-300微米时,及时解离并重新接种对于持续扩增至关重要。若允许类器官生长超过推荐的尺寸范围,尤其是具有实性形态的类器官培养物将变得难以成功解离,从而抑制后续的细胞生长。对培养物进行频繁成像,特别是在研究人员逐渐熟悉患者来源细胞系的形态和生长速度时,对于实验成功至关重要。当遵循以下所述的最佳喂养和传代操作规范时,类器官的生长速率、基因型和基因表达可在培养中保持稳定250天以上。
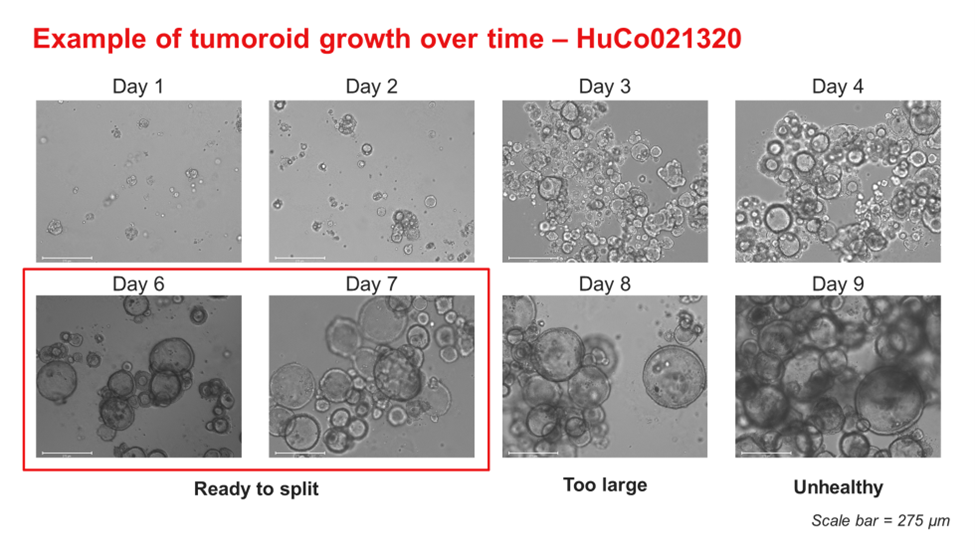
图1:HuCo021320结直肠类器官在OncoPro类器官培养基(悬浮培养格式,囊性形态)中的生长时间过程图像。如果类器官生长超过推荐尺寸范围,则会如第9天所示出现暗色和坏死区域。
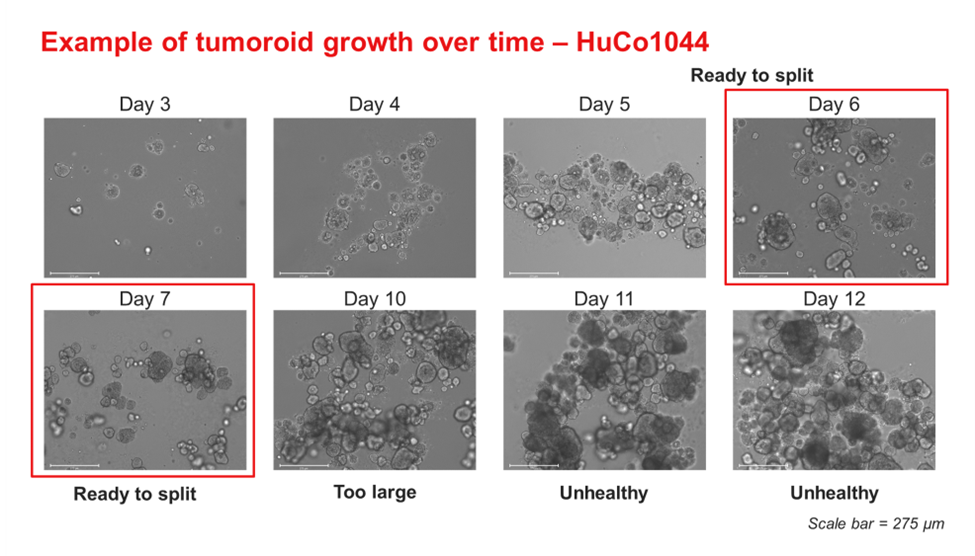
图2:HuCo1044结直肠类器官在OncoPro类器官培养基(悬浮培养格式,实性形态)中的生长时间过程图像。如果类器官生长超过推荐尺寸范围,则会如第11-12天所示出现暗色和坏死区域。
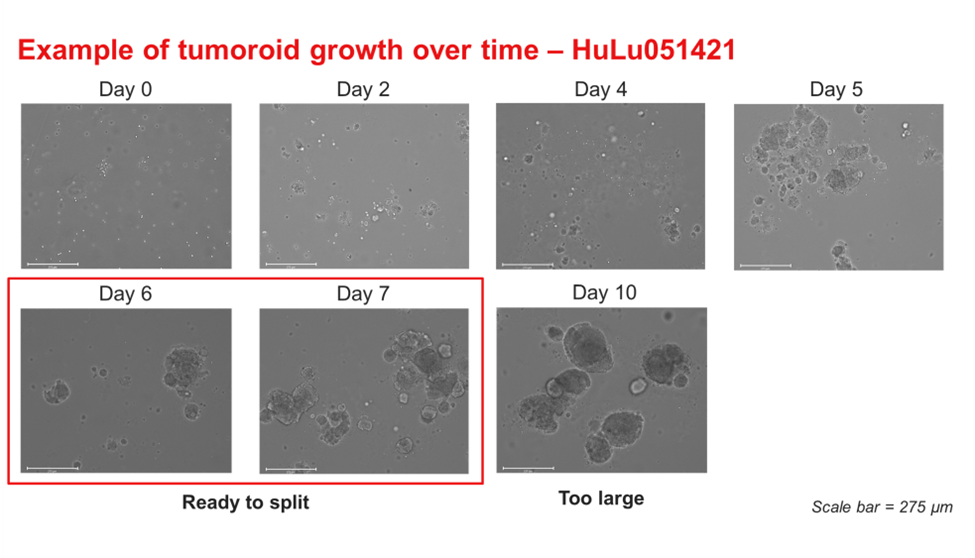
图3:HuLu051421肺部类器官在OncoPro类器官培养基(悬浮培养格式,实性形态)中的生长时间过程图像。虽然在第10天的图像中未观察到暗色坏死核心,但当直径过大时,类器官可能变得难以解离,并影响后续培养物的健康状况。
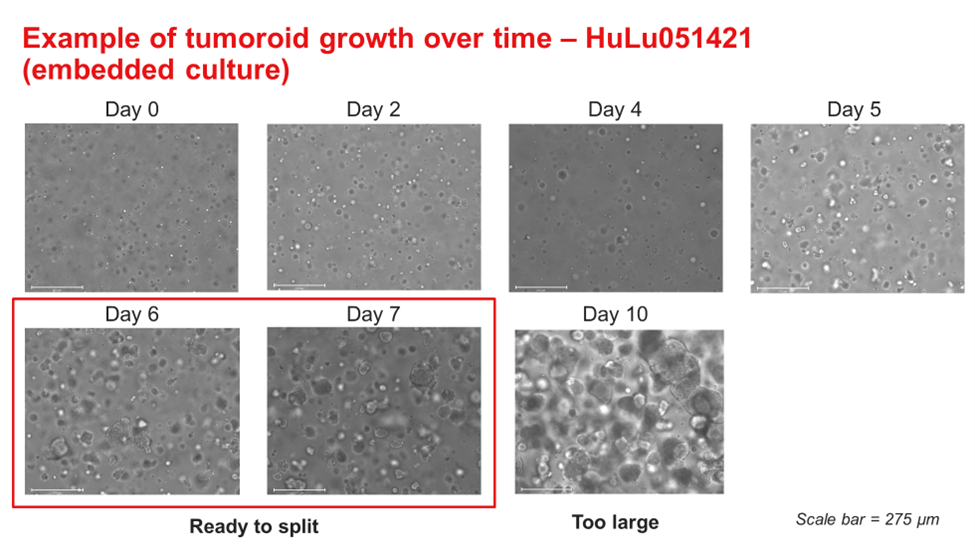
图4:HuLu051421肺部类器官在OncoPro类器官培养基(包埋式培养格式,实性形态)中的生长时间过程图像。虽然在第10天的图像中未观察到暗色坏死核心,但当直径过大时,类器官可能变得难以解离,并影响后续培养物的健康状况。
类器官培养最佳实践指南
以下提供了一些建议,以帮助您在不同阶段最大化提升类器官工作流程中的培养成功率。
类器官培养基制备
- 使用OncoPro肿瘤类器官培养基套装:OncoPro肿瘤类器官培养基经过优化,适用于扩增患者来源的肿瘤类器官。OncoPro套装简化了癌症类器官培养基的制备流程,无需重新配制、分装和混合常见于自制类器官培养基中的各类生长因子和补充剂。
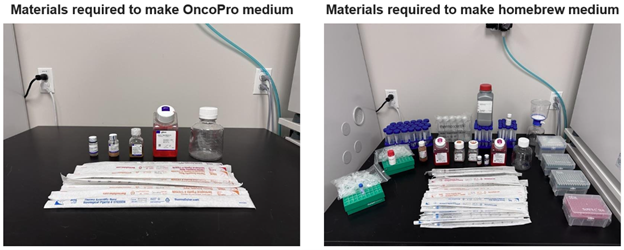
图5:准备OncoPro肿瘤类器官培养基(不含抗生素)及代表性自制培养基所需的材料。对于自制培养基,展示了重悬、分装及储存各个生长因子和补充剂所需的材料。
- 培养基组分的储存:如有需要,当每次使用量少于500毫升时,可将OncoPro肿瘤类器官培养基组分进行分装。OncoPro基础培养基和OncoPro BSA应储存在4°C,可直接从原始组分瓶中取用。B-27补充剂可在室温下解冻,分装后再次冷冻并储存于-20°C。OncoPro补充剂应在37°C水浴中解冻,分装后快速冷冻于-80°C过夜,然后储存于-20°C。各组分的分装品可保存至其有效期。不建议将完整培养基配好后再冷冻保存。
- 培养基制备频率:请配制完整培养基,并在7天内使用以获得最佳效果。不使用时,将其储存在4°C并避免光照。
- 使用前加温处理:避免使用37°C水浴加温。如需加温已配好的培养基,建议将其置于室温下(实验台或生物安全柜内)约1小时,并避免光照。不使用时,将其储存在4°C。
癌细胞播种
解离后的肿瘤类器官细胞可以在水凝胶(例如,Geltrex)中进行嵌入式培养,也可以在悬浮培养中进行,此时会向培养基中添加稀释的基底膜提取物(例如,体积比为2%的Geltrex),以提供细胞外基质信号。
- 悬浮培养与嵌入式培养:在初始肿瘤类器官衍生过程中通常更倾向于采用嵌入式条件培养(详见我们的衍生应用说明获取更多信息),而悬浮培养则便于实验规模化扩增。在悬浮状态下的培养可能需要更频繁地分割,因为自由漂浮的肿瘤类器官聚集会导致其形成较大的类器官速度快于嵌入式培养(参见上方图3和图4中HuLu051421肿瘤类器官系在悬浮与嵌入式培养中的对比)。
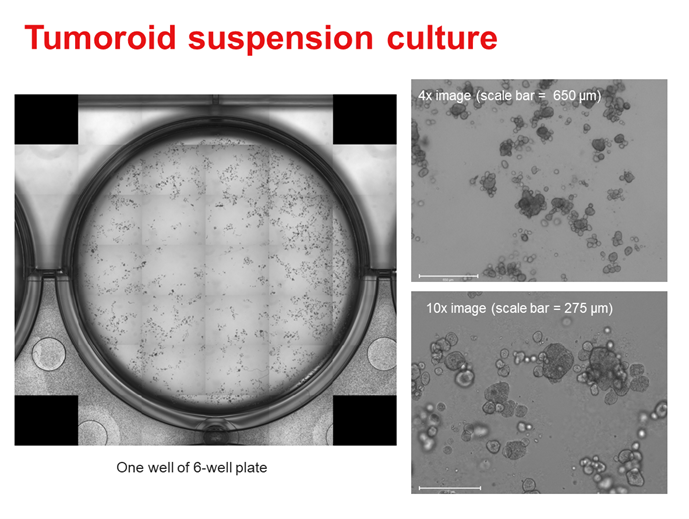
图6:HuCo1044结直肠肿瘤类器官在OncoPro Tumoroid Culture Medium(悬浮培养格式)中播种后第7天,在不同放大倍数下的图像。在悬浮培养中,肿瘤类器官在介质中自由漂浮时形成三维细胞结构。
- BME的添加:在悬浮培养中使用2%(v/v)溶解的BME,以维持具有生理相关性的细胞-ECM相互作用。这些相互作用对于维持肿瘤类器官的顶端-基底极性至关重要。为了获得最佳效果,应在将细胞和介质加入到培养容器后,将冷BME滴加到介质中。
- ROCK抑制剂的使用:在初始播种时,在培养基中补充10 µM Y-27632,以支持单细胞的健康。我们通常在肿瘤类器官培养过程中持续添加该化合物,但在播种后2-3天进行培养喂养时更换培养基,可以选择不再添加。
肿瘤类器官喂养
应定期喂养肿瘤类器官,以去除代谢废物并提供生长所需的营养。在包埋培养中,通过移除用过的培养基并覆盖新鲜的OncoPro肿瘤类器官培养基来进行喂养。在悬浮培养中,将细胞和培养基从板或瓶中取出并离心,弃去上清液,然后将肿瘤类器官重新悬浮于新鲜培养基中。
- 喂养频率:建议每2-3天进行一次完全更换培养基,以确保最佳生长。如果未能每2-3天更换,代谢废物积累会对细胞活性产生负面影响,并可能导致整个培养崩溃。我们建议在喂养或传代当天新鲜补充10 µM Y-27632至培养基中。
- 监测培养基颜色:OncoPro肿瘤类器官培养基因其略酸性的pH值,颜色可能比其他培养基更偏黄。随着肿瘤类器官扩增并代谢介质成分,介质会进一步酸化,当细胞接近传代时,介质看起来尤其偏黄。需要频繁监测(每2-3天)以判断何时分割培养。如果已定期更换介质且肿瘤类器官直径处于100-300 µm范围内,则黄色不是值得担忧的问题。

图7:肿瘤类器官培养中的介质颜色示例。图中为三只T25瓶,在喂养后2-3天拍摄,都含有正常扩增的肿瘤类器官。当肿瘤类器官数量和体积增加、接近传代时,介质可能变得更加偏黄。
- BME补加:在悬浮培养过程中,一部分BME会在肿瘤类器官喂养时流失。为补充丢失的BME并保持其益处,可加入1%(v/v)的BME(如Geltrex)在每次换液时加入培养基中。BME应在细胞和培养基接种到培养容器后再添加,而不是在喂养过程中与细胞预先混合于锥形管中。
癌类类器官的传代
鉴于不同供体之间形态各异,密切监控肿瘤类器官的培养过程至关重要,尤其是在初期阶段。由于不同的肿瘤类器官具有独特的形态并以不同速度扩增,监测有助于最大化成功率,并为何时进行亚培养提供关键信息。
- 传代的最佳直径:我们建议当培养中的大型肿瘤类器官直径达到100–300微米时进行传代(通常每6-10天一次,但部分培养物可在5–14天内分割)。大多数肿瘤类器官系在准备亚培养时直径可达200-300微米,但某些系可能仅生长至约100微米。过早传代会对存活率产生负面影响,并导致过度解离为单个细胞,从而增加失巢凋亡(anoikis)的风险。延迟传代则可能导致坏死核心形成、解离效果不佳、代谢废物积累以及最终的培养崩溃。下图中的肿瘤类器官代表了同一癌症类型(本例为结直肠癌)内可能出现的形态变化。
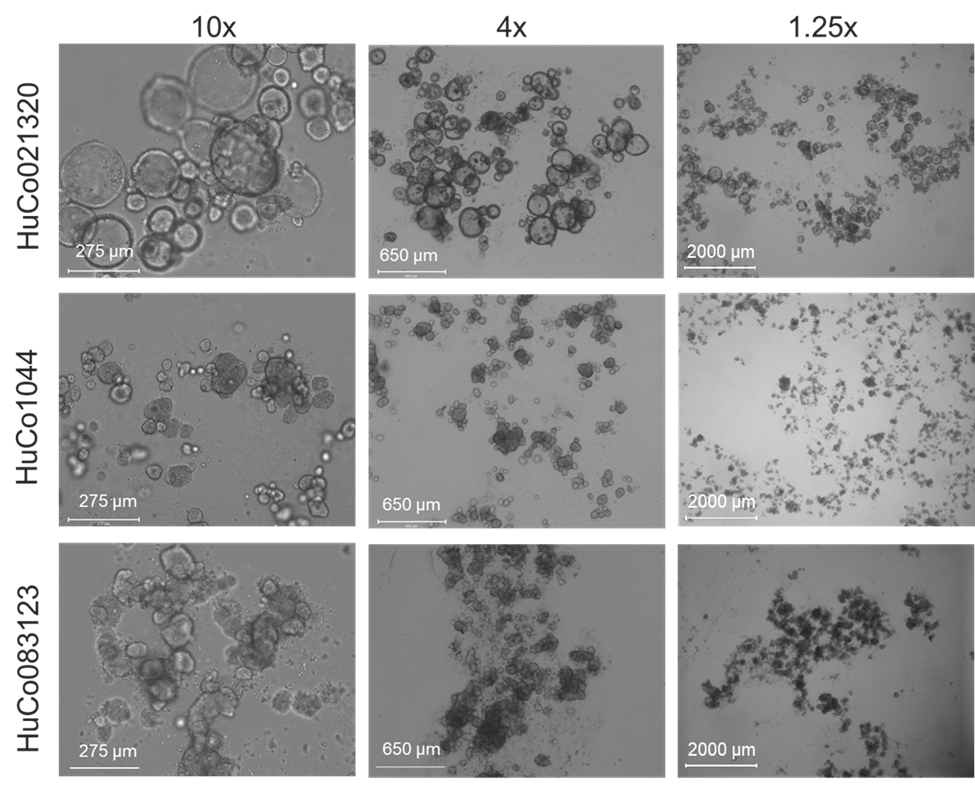
图8:三种结直肠癌肿瘤类器官系在10倍、4倍和1.25倍显微镜下准备传代时的代表性图像,比例尺已标注。
- 洗涤步骤:使用冷缓冲液(如冷DMEM/F12、DPBS -/-)打散聚合后的BME,并将细胞从BME网络中分离出来。这一步对于确保消化酶能有效解离肿瘤类器官至关重要。
- 消化试剂:根据我们的经验,使用StemPro Accutase进行分离能够获得稳定的生长速率。这种酶能够高效地将肿瘤类器官解离为单个细胞和小型细胞团,同时不会影响细胞活性。StemPro Accutase等分试剂应储存于-20°C,并在使用当天于室温下解冻。其他解离试剂如TrypLE也可根据研究的具体需求和类器官模型的特性选择使用。我们建议在孵育过程中向解离试剂中补充10 µM Y-27632,以支持单一化肿瘤类器官细胞的健康。
- 解离温度:我们建议在37°C条件下,用补充了10 µM Y-27632的StemPro Accutase对肿瘤类器官进行解离。此操作可在37°C水浴中进行,也可将CO2耐摇床放置于37°C、5% CO2细胞培养箱内,并设置为120 rpm。不建议使用加热珠浴进行解离。在水浴中进行解离时,每2-3分钟轻轻旋转含有肿瘤类器官悬液的锥形管,以保持其在解离试剂中的均匀分散。
- 吹打:经过与解离试剂孵育后,用P1000移液器吸头将细胞悬液反复吹打20次,以进一步分散肿瘤类器官。不要使用宽口移液器吸头,因为它们无法提供足够的机械力来破坏三维结构。在此步骤之前,移液器吸头应预先润湿(通过吹打无细胞的OncoPro肿瘤类器官培养基),以避免细胞粘附在吸头上。当用P1000移液器吸头吹打后,细胞溶液变浑浊即表明解离充分。肉眼不应看到任何细胞团块,且在传代后不应有边界清晰、完整的肿瘤类器官残留。

图9:锥形管内有效解离的肿瘤类器官(上)和需要在StemPro Accutase中延长孵育时间的肿瘤类器官(下)的图片,这些可用肉眼观察到。
- 延长孵育:如有疑问,可在解离试剂中再孵育5-10分钟,并再次吹打,然后稀释并计数。我们建议每次增加2分钟解离时间,总时长最多可达20分钟,直到细胞充分解离为止。
- 难以解离的细胞系震荡处理:对于特别难以有效解离的细胞系,可以考虑在与解离试剂孵育期间,每两分钟对封闭管进行短暂震荡(例如使用FisherbrandTMMini Vortex Mixer震荡2秒)。
- 细胞计数:我们建议每次传代都进行细胞计数,以更好地控制播种的一致性,并量化各模型的倍增时间及累计群体倍增数。在计数过程中,可能会出现小型细胞团块。为了获得准确数据,应计入这些团块中的单个细胞(见图10)。可以在基于图像的自动化细胞计数仪上实施去团算法,以准确计数小团块中的细胞。我们发现,将最小物体直径设为8微米、最大物体直径设为60微米,并采用基于图像自动化计数仪上的最高去团程度,可以获得准确的细胞计数数据。
- 细胞在传代过程中的存活率:肿瘤类器官的细胞存活率具有变异性,并且不同供体之间可能存在显著差异。解离后,肿瘤类器官的存活率(通过台盼蓝排除法)通常在65-90%之间。虽然这些存活率低于永生化细胞系通常观察到的水平,但它们应在多次传代过程中保持稳定,并不一定表示培养中细胞健康状况较差。
解离后,培养物应由单个细胞和小型细胞团混合组成,如下图所示。
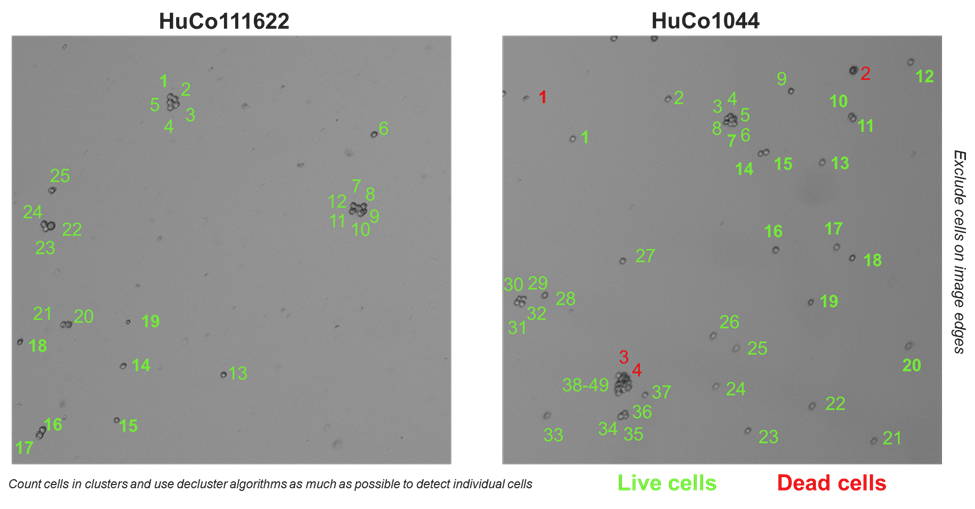
图10:肿瘤类器官解离后的代表性图像,绿色为存活细胞,红色为死亡细胞。在计数时,应尽量统计聚集中的单个细胞,以获得最准确的细胞数量定量结果。
癌症类器官培养的其他注意事项
- 悬浮培养期间的细胞黏附:某些肿瘤类器官天生“黏性”较强,在悬浮培养过程中可能会黏附于非组织培养处理过的瓶壁。如果发现某一肿瘤类器官系出现黏附现象,可在播种前,将孔板或瓶用7.5% BSA溶液(用无钙、无镁DPBS稀释)在37°C细胞培养箱中涂覆30分钟。BSA溶液可在加入肿瘤类器官悬液(使用OncoPro Tumoroid Culture Medium)进行初次播种或换液后立即吸出,无需进行中间清洗步骤。
- 包埋培养期间的细胞黏附:在某些情况下,在BME水凝胶中培养时可能会观察到细胞黏附和扩展。为减少细胞对细胞培养塑料的黏附,可以使用非组织培养处理的孔板和培养皿。如果操作得当,水凝胶穹顶在初始细胞接种过程中倒置以聚合BME时,会保持在这些容器上。如有需要,收集BME穹顶中的肿瘤类器官细胞后,可使用TrypLE或类似解离试剂分离贴壁细胞。
- 血清移液管和移液枪头预湿:我们建议在处理肿瘤类器官前预先湿润血清移液管和移液枪头,以减少细胞/肿瘤类器官对培养塑料的黏附及随后的细胞损失。对于允许操作过程中丢失部分细胞的工作流程,预湿可能不是必需的。
利用OncoPro肿瘤类器官培养基推动癌症研究进展
癌症类器官模型提供了一个强大的平台用于研究肿瘤生物学。通过理解并利用癌症类器官,研究人员能够推动癌症领域的发展,并助力更有效治疗方法的开发。定期成像、持续喂养以及适当传代是确保这些三维模型存活与稳健的关键实践。详细协议、推荐细胞密度及培养基体积已包含于OncoPro肿瘤类器官培养基用户指南。
注:部分图片改编自Paul, C.D. 等人 bioRxiv 10.1101/2024.06.10.598331v1 (2024)。
相关内容
仅供科研使用。不用于诊断程序。



发表回复