作者:John Pfeifer
实时荧光定量PCR(聚合酶链式反应)是一种在每个PCR循环后检测特定基因序列扩增的技术。这项技术可以用于检测或定量多种应用中的基因序列。
实时荧光定量PCR分析包括一组寡核苷酸,用于扩增和检测特定的基因靶标。实时荧光定量PCR分析通常由两个PCR引物和一个带有荧光标记的探针组成,这种探针被称为TaqMan探针。
实时荧光定量PCR测试或实验通常设定为运行40个循环,但高价值的数据只涵盖少数几个循环,并且这些循环在不同样本之间可能有所不同。如何从实时荧光定量PCR数据中筛选出高价值的数据点?
扩增曲线图
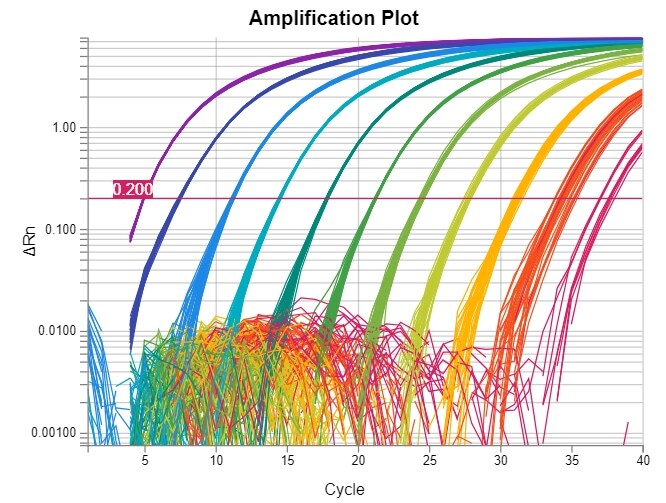
实时荧光定量PCR数据通常以一种称为扩增曲线图(见图1)的方式表示。纵轴单位为荧光值,测量值常被称为ΔRn,即经过基线扣除并标准化后的报告信号。横轴则表示PCR循环次数。
基线定义为早期PCR循环中,在扩增信号尚未可检测到之前的数据。在纵轴采用线性刻度的扩增曲线图中,基线应表现为一条平直的线。在基线周期内,目标基因可能已经开始扩增,但报告信号(如来自TaqMan探针)尚未积累到足以被观测到的程度。如果反应体系中存在目标序列,最终扩增信号将会从基线上升出来。
图1
基因定量
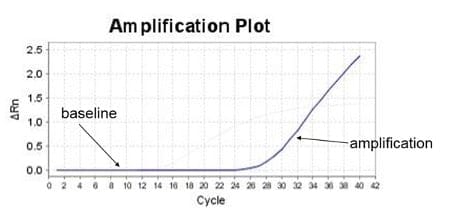
实时荧光定量PCR是基因定量的金标准。其原因在于指数期扩增具有极高的一致性。指数期(也称为几何期、对数期)是PCR的第一个阶段,此时所有反应物——如引物、DNA聚合酶、dNTP等——都处于过量状态,从而保证了扩增效率的一致性。这种一致性意味着,PCR反应中初始目标基因的数量将决定扩增信号何时从基线中显现,如图2所示。起始目标数量越多,扩增信号出现得就越早。
每个扩增曲线需要一个高价值的数据点来计算初始目标数量值。基线数据点没有定量价值。指数期的数据点价值最大。当某一反应物不再足以维持一致效率时,指数期结束,随后的数据点价值降低。因此,需要一种方法,在一致的位置选择指数期数据点,以便在同一次实验中具有可比性。
图2
Ct值
从实时荧光定量PCR扩增曲线获得的单个数据点被称为阈值循环或“Ct”(也称为Cq)值。最早且仍然最常用的Ct值产生方法被称为基线-阈值法。
在所有实时荧光定量PCR化学体系中,总会存在一定的基线荧光,并且不同孔之间可能略有差异。通过实时荧光定量PCR软件中的基线扣除算法,这种差异大大减少,该算法将所有基线设定为约零。通过将所有基线设为零,阈值就能从统一的起点设置。
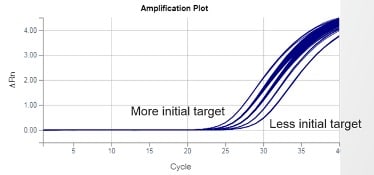
阈值是针对某一实验选定的荧光值(ΔRn),用于计算Ct值。阈值通常设置在PCR的指数期内。在放大曲线上,用对数坐标y轴最容易识别出指数期,此时各条曲线表现为斜率相同的平行直线(见图3)。在扩增曲线上,阈值表现为一条水平直线。
阈值与扩增曲线相交的位置即产生Ct值。Ct值通常不是整数。
图3
定性结果
Ct值可用于定性检测,例如判断病原体的存在或不存在。没有Ct值意味着该反应中未检测到目标物,出现Ct值则表示目标物存在。
定性检测通常包含一个对照基因,用于质量控制。如果对照检测的Ct值过高,则目标阴性样本结果的有效性将受到质疑。例如,可能在样本采集、提取过程中出现了问题,或者存在抑制剂等情况,这些都可能导致检测灵敏度低于可接受水平。
对于定性检测,为了保证每次实验运行时Ct值计算的一致性,阈值通常是固定的。
定量结果
定量结果有多种类型:相对与绝对,以及数量与浓度。在实时荧光定量PCR软件中,“quantity”(数量)一词被广泛用于涵盖所有这些结果类型。
实时荧光定量PCR中的绝对定量是指确定目标分子的实际数量或浓度;而相对定量则是用非分子或任意单位来确定数量。
不建议将Ct值作为最终的定量结果进行报告,因为Ct值是抽象、不完整且数学上较为复杂的数据。仅有Ct值在定量上是不完整的,因为其定量解释依赖于指数阶段效率。例如,Ct标准差并不像普通标准差那样表现。
定量结果应以“数量”形式报告,这是一种完整且数学上更简单的数据点。“数量”可以通过Ct值和指数阶段效率计算得出:
公式1
Quantity ~ e-Ct
Where:
数量 = 初始目标基因数量
e = 指数期效率,理想值为2(目标每个循环翻倍)
Ct = 阈值循环数
涉及生物样本的实时荧光定量PCR定量通常包括一个标准化基因。该基因用于测量样本质量,并通过样本质量对目标量进行归一化,以获得具有生物学意义的目标浓度。
校准是定义数据集单位的一种方法。在实时荧光定量PCR中,一个常见做法是使用某个样本或一组样本的平均值作为“校准器”(也称为参考样本或参考组)。校准器样本或组的相对数量(RQ)设为1,其他所有样本的RQ值都以此为参照。校准器可以是相对的,也可以是绝对的。
在1997年名为“用户公告#2”的文件中,方程1被修改用于样本质量归一化和校准,并将指数效率设定为100%。由此得到的公式被称为比较Ct或ΔΔCt方法:
方程2
相对数量 = 2-ΔΔCt
Where:
ΔΔCt 是通过样品质量归一化并校准后的 Ct 值。
注意,Ct 值的归一化是通过减法而不是除法进行的,符号 Δ 表示减法。
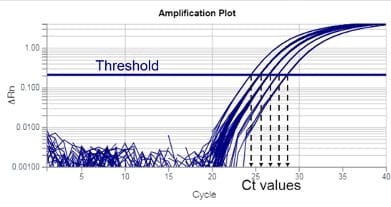
对于定量检测,可以在指数阶段的 ΔRn 值范围内设置阈值(见图4)。在以对数 y 轴显示的扩增曲线中,指数阶段结束于曲线开始向右弯曲的位置。由于精确度降低,阈值不应设置在该弯曲区域。此外,阈值也不应设置得过低,否则数据会表现出更大的变异性。这种变异性是由信噪比低造成的。
调整阈值会改变该检测的 Ct 值,但如果阈值设置在推荐范围内,则 Ct 值变化是一致的。在使用 ΔΔCt 方法时,一致的 Ct 值变化不会显著影响最终结果数量。
不同检测之间不要求使用相同的阈值,但如果每个检测都适用,该阈值也可以为了方便设为相同。
建议通过扩增曲线图对阈值进行目视评估,以确保其处于可接受范围,即使采用自动阈值算法也是如此。图4
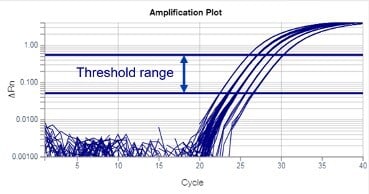
相对阈值法
一些实时荧光定量PCR软件程序提供了一种计算Ct值的替代方法,称为相对阈值法。该方法是自动化的,因此无需评估或修改基线或阈值设置。该算法会识别可能的扩增信号,并根据每个扩增曲线的形状在一致的位置计算Ct值。使用相对阈值法时,Ct值将在软件中显示为“Crt”值,以标识所采用的方法。
实时荧光定量PCR软件会计算质量控制数值,这些数值可能包括Cq置信度、扩增评分和扩增状态。建议评估这些质量控制数值,以确保Ct这些数值来自真实的扩增反应。
等效Ct值
除了Ct值之外,一些实时荧光定量PCR软件程序还会显示“等效”Ct值,即如果检测具有100%指数期效率时应有的Ct值。如果检测效率在软件中保持默认的100%,则Ct值与等效Ct值将完全一致。
只有在极其谨慎的情况下才应将检测效率从默认的100%更改。常见的一种计算指数期效率的方法是基于标准曲线斜率,但标准曲线斜率会随机波动。建议仅使用具有100%指数期效率的检测进行实时荧光定量PCR,因为低效率检测会带来不必要的复杂性。例如,如果某一检测效率较低,则准确测量其效率将变得困难。此外,为了保持灵敏度,实时PCR常规使用的40个循环次数也需要增加。
本文仅浅析了实时荧光定量PCR(qPCR)的基础内容。如需了解更多信息,请访问以下有用资源:
- 理解Ct应用说明
- Taq Talk 视频,第3集:理解Ct实时荧光定量PCR中的数值
- Taq Talk 视频,第12集:实时荧光定量PCR中的基线
- Taq Talk 视频,第13集:实时荧光定量PCR阈值及其设置位置
- Taq Talk 视频,第14集:如何判断Ct值是真实信号还是背景噪音
- qPCR手册2.0,数字体验




发表回复