
提取高质量、完整的基因组DNA是许多后续分子应用的基础步骤——但并非所有DNA都是一样的。高分子量(HMW)DNA的提取对于实现依赖于长且未碎片化DNA链的高级基因组分析至关重要,尤其是在结构变异检测、基因组组装和表观遗传分析中。
随着长读长测序技术的兴起,能够稳定地分离出大于40 kb、甚至超过100 kb的DNA片段已不再是奢侈,而成为尖端基因组科学的必需条件。
理解DNA的复杂性对于基因组学和生物技术的发展至关重要。诸如基因组DNA、高分子量DNA以及创新性的长读长测序技术等基本概念,通过使无参考组装成为可能,彻底改变了de-novo测序的效果。在本文中,我们将深入探讨不同类型基因组DNA结构,包括高分子量DNA,并分析它们如何影响长读长与短读长测序,揭示其独特应用和优势。
目录
什么是基因组DNA?
基因组DNA(gDNA)指的是一个生物体内的全部DNA,包括所有基因和非编码区域。基因组DNA通常可用于分子应用,如PCR、测序和下一代测序。
什么是高分子量DNA?
高分子量(HMW)DNA特指那些极其长且完整的DNA分子,通常长度从数百千碱基到百万碱基不等。虽然gDNA包含所有遗传物质,但HMW DNA以其较大的尺寸和高度完整性为特点,使其在需要长、连续DNA链进行准确分析和组装的应用中(如长读长测序和全新基因组组装)尤为重要。
长读长与短读长测序:有什么区别?
短读长和长读长方法主要区别在于它们能够分析的DNA片段长度。
短读长测序
短读长测序
——最常用的大规模并行测序或下一代测序(NGS)形式——是一种广泛采用的方法,能够生成数百万到数十亿个通常长度为50至300个碱基对的DNA片段。由于其高通量、每碱基低成本以及成熟的信息分析流程,过去十年里它成为研究与临床实验室主流的测序技术。从RNA-seq到靶向重测序及微生物分析,短读长平台推动了无数生命科学突破。然而,尽管短读长测序在变异检测和定量方面表现出色,但在重复区域、结构变异及单倍型分辨方面存在不足——这些领域正逐渐被更适合的长读长测序所青睐。短读长测序仍然因其可扩展性、可靠性及广泛应用基础而备受欢迎。
长读长测序
长读长测序是一种DNA测序技术,能够产生相对较长的平均读取长度,通常从几千到十几万甚至超过十万碱基对。长读长测序技术在诸如全新基因组组装、结构变异检测以及解决单倍型分型等应用中尤为重要,使得对基因组有更全面的了解。
有什么区别?
长读长测序与短读长测序不同之处在于它能够测序更长的DNA片段(数千到数十万碱基对),而短读长测序则使用较短的片段(通常最多几百个碱基对),这使得复杂基因组区域的组装和分析更加准确。像Thermo Fisher Scientific Ion Torrent Chef/S5系统或Thermo Fisher Scientific Ion Torrent Genexus测序仪这样的短读长测序平台,可以高效地测序大量短DNA片段,非常适合与全基因组测序和靶向测序集成工作流程。下表1概述了短读长和长读长测序技术在多种应用中的一些优势。
比较短读长和长读长测序的优势与应用
| 短读长 | 长读长 | |
|---|---|---|
| 优势 | 高准确性 成本效益 高通量 使用标准基因组DNA | 更长的读取长度 与短读段相比,可能提升结构变异检测能力 可解析复杂区域 使用高分子量基因组DNA(≥ 40 kb)* |
| 结构变异 | 仅限于小型结构变异 | 对大规模基因组改变至关重要 |
| 全新基因组组装 | 对新基因组组装效果较差 | 对于从头组装基因组至关重要 |
| 单倍型分型 | 分型能力有限 | 确定长距离的相位关系 |
| 表观遗传学研究 | 表观遗传分析有限 | 同时进行遗传和表观遗传分析 |
| SNP和小型插入缺失检测 | 非常适合检测SNP和小型插入缺失 | 对非常小的变异效果较差 |
*DNA片段大小的要求根据应用和平台有很大差异
高分子量(HMW)DNA对长读长测序的重要性是什么?
高分子量基因组DNA(HMW gDNA)用于长读长测序以及其他需要大分子DNA的应用,如光学基因组图谱。由于去 novo 测序和长读长测序应用需要高分子量DNA的复杂性,对于大多数应用来说,拥有高质量且大于40kb的分离DNA至关重要。在某些情况下,拥有大于100kb的DNA可以获得更优结果。评估或实验室生成过程中,兼顾通量需求、质量和基因组大小可能会带来困难。
高分子量DNA提取
Applied Biosystems™ MagMAX™ HMW DNA Kit 旨在获取适用于Oxford Nanopore或PacBio等制造商的长读长测序平台所需的高分子量基因组DNA。MagMAX HMW DNA试剂盒经过优化,可从新鲜或冷冻全血、培养细胞和组织中获得高质量产量和性能表现。
该试剂盒采用磁珠技术,并针对手动分离流程或使用Thermo Fisher Scientific KingFisher™纯化仪自动化流程进行了优化,实现了样本通量和实验室自动化需求的灵活性。
MagMAX HMA DNA试剂盒的性能数据可在线获取包括DNA产量、质量、片段大小以及按样本类型进行的片段回收。
了解常见的高分子量DNA提取挑战
以下是一些在分离高分子量基因组DNA时可能遇到的挑战示例。我们提供了可能的解决方案,以帮助提升提取质量、效率及后续应用中的表现。
1. 产量低的样品
MagMAX HMW DNA试剂盒设计用于从200uL新鲜/冷冻全血、1 X 106个细胞以及最多8mg组织中获得至少3微克高分子量基因组DNA。A260/280和260/230比值大于1.8为最佳,以确保蛋白质和污染物携带最小化。
低产量和纯度可能由下述所有样本类型中的多种原因造成,详见下文说明。
所有样本类型的产量较低
可能原因:DNA样品在工作流程中丢失。
解决方案:如果进行手动分离,移液器吸头可能会留下微量样品。在丢弃前请务必检查移液器吸头。在使用手动流程进行分离时,高分子量基因组DNA在洗涤步骤中可能会缠绕在吸头上。
可能原因:混合不充分。
解决方案:如果在裂解/结合或洗涤步骤中观察到大段基因组DNA缠绕在磁珠上,在使用手动流程时,请务必用常规孔径的移液器吸头将其打散。将高分子量基因组DNA-磁珠团混合5-10次即可,避免过度混合以防止过度剪切。建议使用KingFisher纯化仪上的自动化流程,以消除混合一致性方面的人为错误。KingFisher纯化仪已验证能以用户说明中的既定混合速度实现最佳性能。
可能原因:磁珠过度干燥。
解决方案:如果磁珠在50°C下干燥2分钟后出现裂纹,建议在使用手动流程时于室温下空气干燥磁珠2分钟。可考虑采用优化后的KingFisher纯化协议,以消除干燥一致性方面的人为错误。
可能原因:样品消化不足。
解决方案:请根据MagMAX HMW试剂盒用户指南中针对每种具体样品消化需求的建议操作,避免样品过量。请注意,MagMAX HMW试剂盒中的增强溶液可以提升蛋白酶K的活性,但在低温下也可能发生沉淀。如果增强溶液出现沉淀,请确保在使用前于37°C孵育,以保证最大效率。建议使用KingFisher纯化仪进行分离,因为其加热板可提供持续且充足的热量,从而确保按照验证过的MagMAX HMW流程获得适当消化效果。
全血样品产率低
可能原因:血液中含有血红蛋白和其他蛋白质,这些成分难以彻底洗净和充分消化。
解决方案:在手动操作流程中,第三次洗涤后务必将样品转移到新的管中,以防止污染物随洗脱液带入。建议使用KingFisher纯化仪上的自动工作流程,这不仅能减少因操作者引入的样品间交叉污染风险,还能帮助确保从结合、洗涤、干燥到核酸洗脱过程的一致性分离效果。
可能原因:起始样品白细胞(WBC)计数较低或起始样品已凝块
解决方案:白细胞计数低意味着用于DNA提取的细胞数量较少,从而导致总体DNA产量降低。血液凝块会使核酸,尤其是高分子量基因组结构难以分离。为避免血液凝块,请保持最佳存储条件、使用血液稳定剂(如K2EDTA),并避免在处理前过度混合样品。
培养细胞样品产量低
可能原因:分离超过100万培养细胞
解决方案:MagMAX HMW DNA试剂盒经过优化,可处理最多100万培养细胞。如果尝试处理超过100万培养细胞,建议将所有组分的试剂体积按线性比例增加。在手动操作流程中,请确保使用适当的工作溶液容器,以容纳所用试剂体积。对于自动化KingFisher操作流程,建议利用 BindIt软件(用于KingFisher Flex纯化系统、KingFisher Duo Prime纯化系统)或BindIx软件(用于KingFisher Apex纯化系统),以反映新的工作体积条件。请注意,96磁头最大允许体积为1mL,而24磁头最大工作体积为5mL。Thermo Fisher Scientific尚未验证超过100万培养细胞或更大规模体积格式的操作流程。
组织样品产量低
可能原因:消化不足可能导致未消化的组织块在洗涤步骤中被带入后续操作。
解决方案:请务必遵循用户指南中列出的消化操作流程。从超过推荐质量的组织中进行分离,可能导致样品消化不充分。如果手动分离高分子量DNA,在加入预消化混合液后,将试管倒置5-10次,以确保在消化前没有组织块卡在管盖上。在消化过程中途检查试管,观察是否有未消化的组织。如发现未消化组织,可使用涡旋仪混匀。建议考虑使用KingFisher纯化仪上的自动工作流程,这可能有助于更均匀地消化所用样品。
2. 洗脱液粘稠或呈棕色
在洗脱板(自动提取)或将样品转移到新试管时(手动提取),可能会观察到部分磁珠残留。一些组织,如脾脏,可能含有大量DNA,从而产生更粘稠或呈棕色的洗脱液。少量磁珠残留进入洗脱液一般不会影响后续的分子应用。
如果磁珠残留过多或对您的后续应用造成抑制:
可能原因:样品输入量过高。
解决方案:MagMAX HMW DNA Kit的工作流程说明已按照用户手册中的比例进行了优化。当使用较少或较多样品时,这些比例可能会受到影响,并导致比例不足,尤其是与磁珠表面积相关,这可能导致洗脱液中出现磁珠残留。请根据用户指南确定每种样品类型的最大输入量。如果您的样品类型未列出,请考虑先进行初步滴定实验,以确定最佳输入量。
可能原因:消化不充分
解决方案:确保按照用户指南中指定的顺序添加 MagMAX HMW DNA 试剂盒中的所有组分。如果操作顺序被调整、未达到所需的充分混合,或消化加热不充分,则 DNA 洗脱液可能会变得“粘稠”、浓厚,并且移液可能会变得困难。如果怀疑消化不完全,请考虑延长消化时间。
您可以采取以下几步来帮助减少洗脱液的粘稠度或磁珠残留。
- 使用磁力架去除洗脱液中的磁珠。
将洗脱板放置在96孔磁力架上,以确保所有磁珠都被吸附。小心地将澄清的上清液转移到新的96深孔板或微量离心管中。 - 确保完全消化。
确保蛋白酶K能够彻底消化,有效分解蛋白质。如有需要,可按照手册协议进行额外的离板蛋白酶K消化步骤。 - 请查阅用户协议说明书。
在处理高DNA产量组织时,请遵循用户指南中关于适当组织输入量的建议。
3. 高分子量DNA降解
HMW DNA降解的一个可能原因在于起始样本材料。
请注意过度混合、样本质量差、样本完全消化,或使用物理机械裂解导致回收的DNA被片段化等风险。请考虑以下事项:
- 避免用血清移液管混合新鲜全血样本,因为这可能会导致DNA剪切。相反,应轻轻颠倒全血样本管至少5次,以确保充分均质后再转移到样本板或管中。
- 对于冷冻血液样本,应限制在一次冻融循环内。
- 对于细胞,在加入MagMAX细胞和组织裂解缓冲液后,确保完全均质化。
- 对于组织样本,不要使用机械研磨。应采用温和的酶消化(如蛋白酶K)。
- 手动分离时,请仔细查阅用户指南中关于移液器吸头(普通与宽孔)的说明。
- 将洗脱产物储存在适宜的温度下(短期为4ºC,若48小时内不进行分析则长期为-20ºC)。
- 避免对分离出的核酸进行反复冻融。
HMW DNA提取常见问题解答
HMW DNA分离流程有哪些应用?
HMW DNA分离具有许多后续应用,包括癌症基因组学研究涉及使用无细胞DNA(cfDNA)作为生物标志物。
哪些样本类型适用于MagMAX HMW DNA试剂盒?
该试剂盒支持多种输入:
- 全血(新鲜或冷冻,约200 µL)
- 培养细胞(约1×10^6个细胞)
- 组织(如2–8 mg)
该试剂盒可以与自动化系统一起使用吗?
是的,MagMAX HMW DNA试剂盒兼容KingFisher Duo Prime、Flex和Apex系统。自动化可实现一致的、无需人工干预的工作流程,耗时不到两小时。也提供手动磁性架操作协议。
MagMAX HMW DNA试剂盒最多可以进行多少次反应?
该试剂盒支持手动和自动处理工作流程,最多可进行100次样品制备。
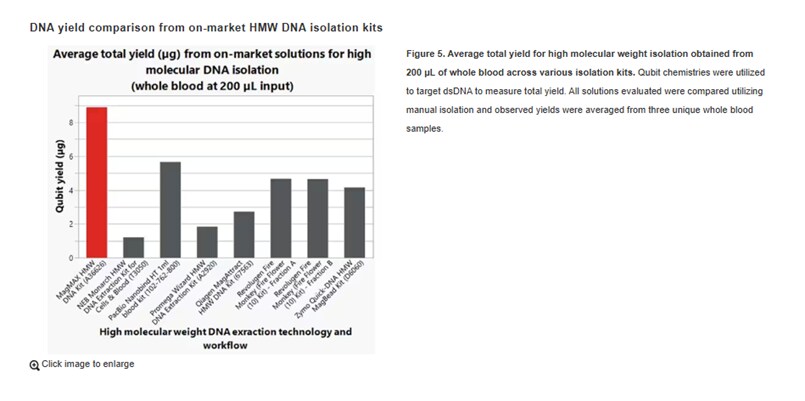
MagMAX HMW DNA试剂盒与其他产品相比如何?
在直接对比中,MagMAX HMW试剂盒从全血中获得的产量与市场上的其他产品相比具有竞争力或表现出色,尤其是在约200微升血液体积时。
使用MagMAX HMW DNA提取试剂盒提取需要多长时间?
自动化工作流程下,提取通常耗时不到2小时。手动操作协议同样快速高效。
关于HMW提取以及长读长和短读长测序的更多资源
- 产品解决方案:MagMAX HMW DNA提取试剂盒
- 用户指南用于提取试剂盒
- 自动化:KingFisher自动化样品纯化和提取系统
- 演示申请自动处理系统
- 了解:测序
##
© 2025 Thermo Fisher Scientific Inc. 保留所有权利。除非另有说明,所有商标均为 Thermo Fisher Scientific 及其子公司的财产。如有说明。
仅供科研使用。不得用于诊断程序。






发表回复