骨髓是造血的场所,可分离出红细胞、粒细胞、单核细胞、树突状细胞、淋巴细胞和造血干细胞等血源性细胞[1]。此外,骨髓也可以作为充质干细胞的来源[2]。分离后的骨髓细胞应用非常广泛,例如直接用于骨髓移植,流式细胞术分析造血干细胞亚群以及各淋巴细胞亚群,或者进行巨噬细胞极化、树突状细胞分化等。那么接下来我们和Dr 赛一起看看怎么得到小鼠骨髓细胞吧!
实验材料
- 细胞培养皿
- 75% 酒精
- RPMI 1640完全培养基(胎牛血清:终浓度 10%;L-Glutamine:终浓度2 mM;可选:1% v/v青霉素-链霉素。)
- 灭菌的眼科剪和镊子(或刀片)
- 1-3 mL 注射器(无菌)
- 25 号针头(无菌)
- 无菌70 μm 细胞筛网
- 无菌50 mL 离心管
- 红细胞(RBC)裂解缓冲液:如果非无菌,建议通过0.22um滤膜除菌
- Invitrogen Countess 3 FL 自动细胞计数仪
- 磷酸盐缓冲液(PBS)
实验步骤
Part Ⅰ 获取股骨
1. 处死小鼠后,用75%酒精充分消毒,在无菌条件下分离小鼠股骨,股骨是位于膝关节与骨盆胯关节之间的长骨 (请参考图一)。
2. 在剥离时,请在骨盆跨关节上方剪下大腿,并在在膝关节下方可活动处剪下股骨下端。注意剥离过程中不要破坏股骨两端关节(请参考图二至图三)。
3. 使用无菌的剪刀,镊子剪掉骨头上的肌肉和纤维组织,整个操作过程留意不要破坏关节或者骨头。可用剪刀刮除骨头表面的肌肉获得如图四所示的股骨。
4. 为获得更多骨髓细胞,可用上述相似的方法获取胫骨内骨髓细胞。
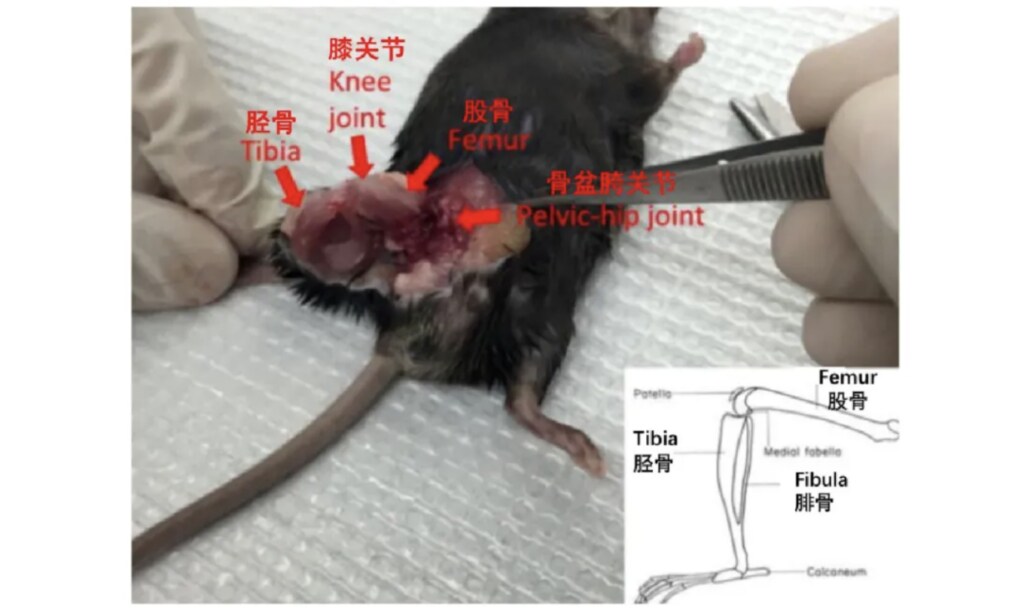
图一:小鼠腿骨简易解剖图
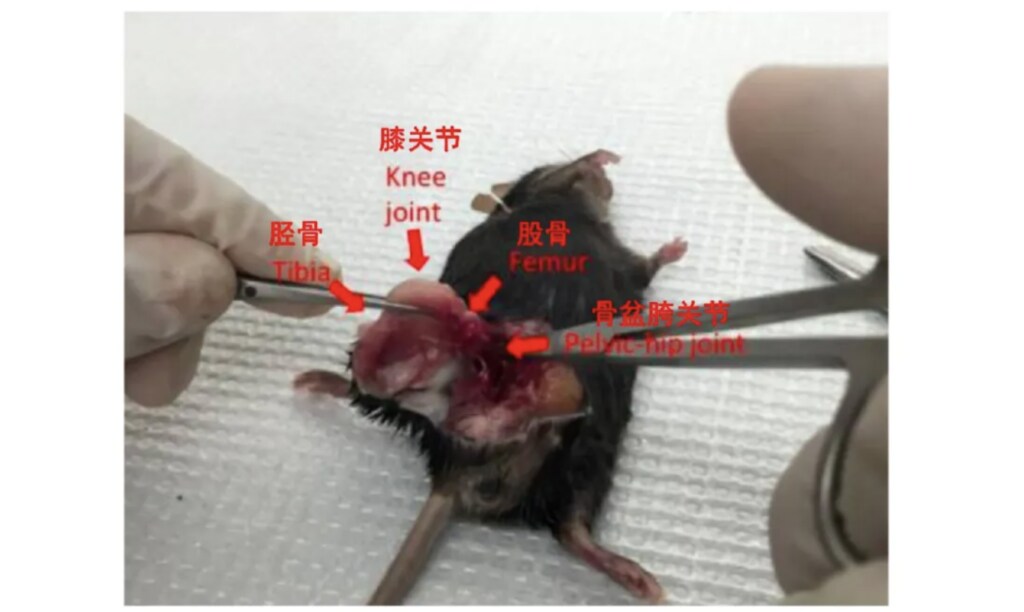
图二:在骨盆跨关节上方剪断大腿
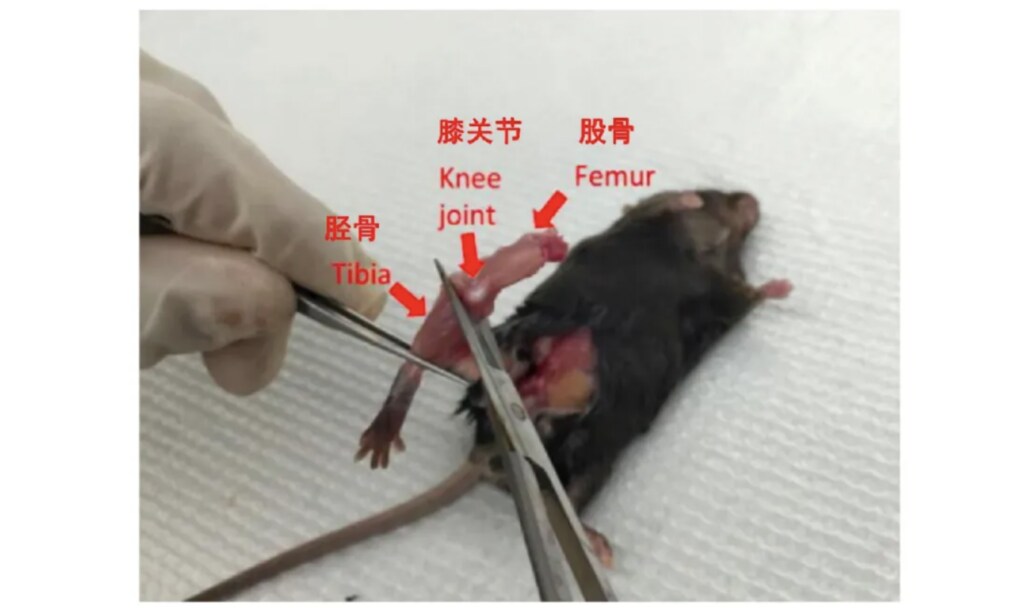
图三:在膝关节下方剪断肌肉/筋膜
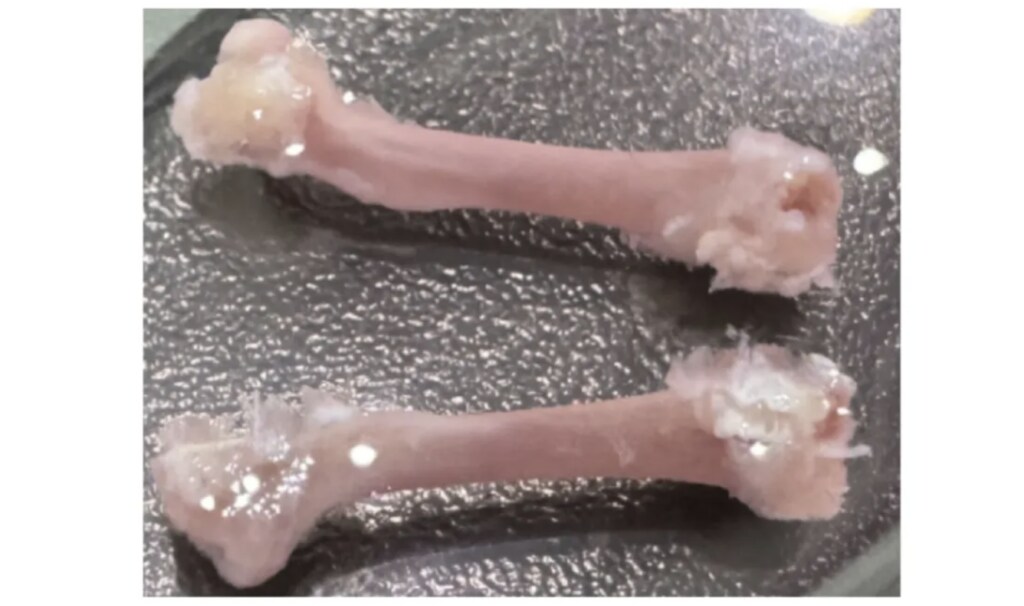
图四:肌肉剥离干净的股骨
Part II 收集骨髓细胞
5. 可将完整的骨头置于培养皿中,使用75%酒精清洗1-2min,再放入含有无菌PBS的培养皿中洗掉酒精。
6. 将 70 µm 细胞筛网置于 50 mL 离心管顶部。
7. 用无菌的眼科剪剪断股骨的两端关节,暴露出骨髓腔(请参考图五),将 25 号针头装在注射器上。用注射器抽吸5 mL左右完全培养基。
8. 用镊子将骨头直立于筛网上方,再用注射器小心将骨髓冲出来(请参考图六)。必要时,重复冲洗,当骨头呈白色则表明已冲出所有骨髓(请参考图七)。对所有骨头重复该步骤。
9. 如果剪掉的股骨关节较大,可进一步用剪刀将其剪碎,并用1mL移液器冲洗。
10. 使用注射器的柱塞(请勿触摸柱塞的黑色橡胶;保持无菌),向下用力顺/逆时针捣碎细胞筛网中的骨髓(请参考图八)。确认骨髓均被捣碎,没有块状。
11. 用 RPMI 完全培养基将柱塞端剩下的骨髓冲到筛网中,尽可能多地收集骨髓。
12. 用完全培养基冲洗筛网。取下筛网,盖上盖子。在 4°C 下 600 x g 离心细胞 4 分钟。丢弃上清液(请参考图九)。
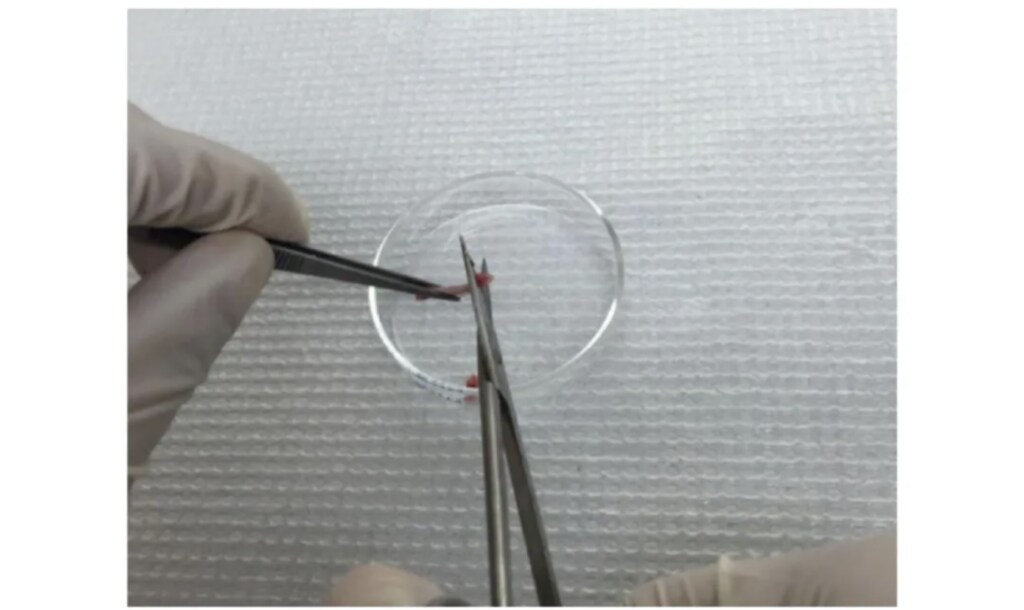
图五:剪掉股骨两端关节
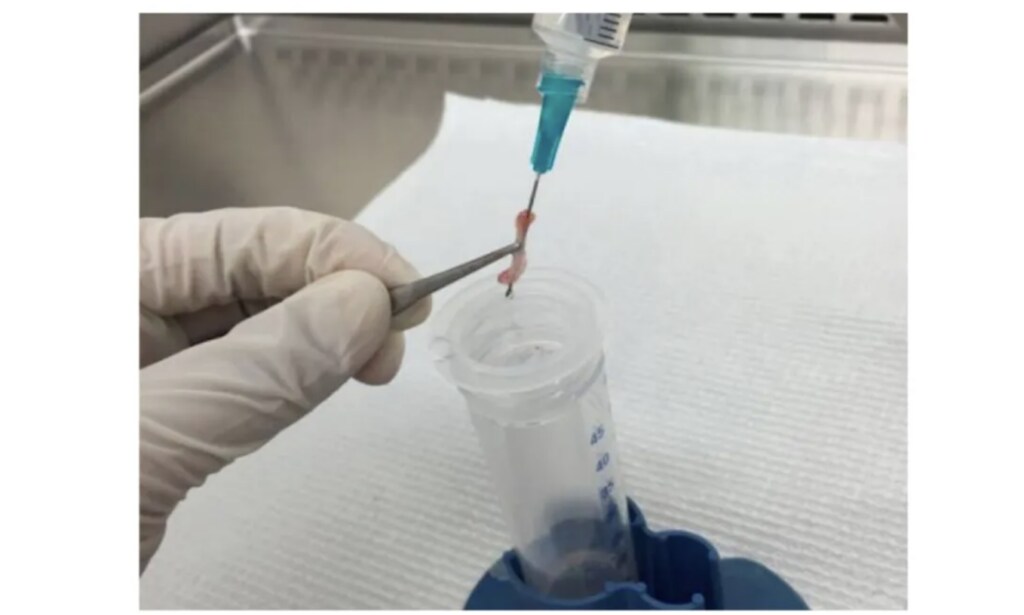
图六:用培养基冲中洗骨髓
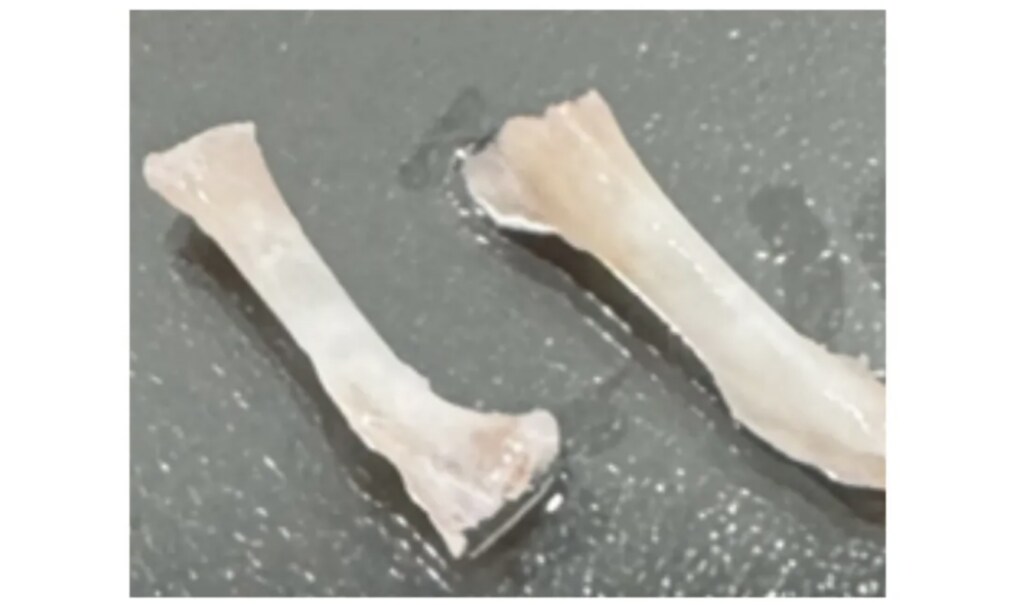
图七:冲洗干净后苍白的股骨
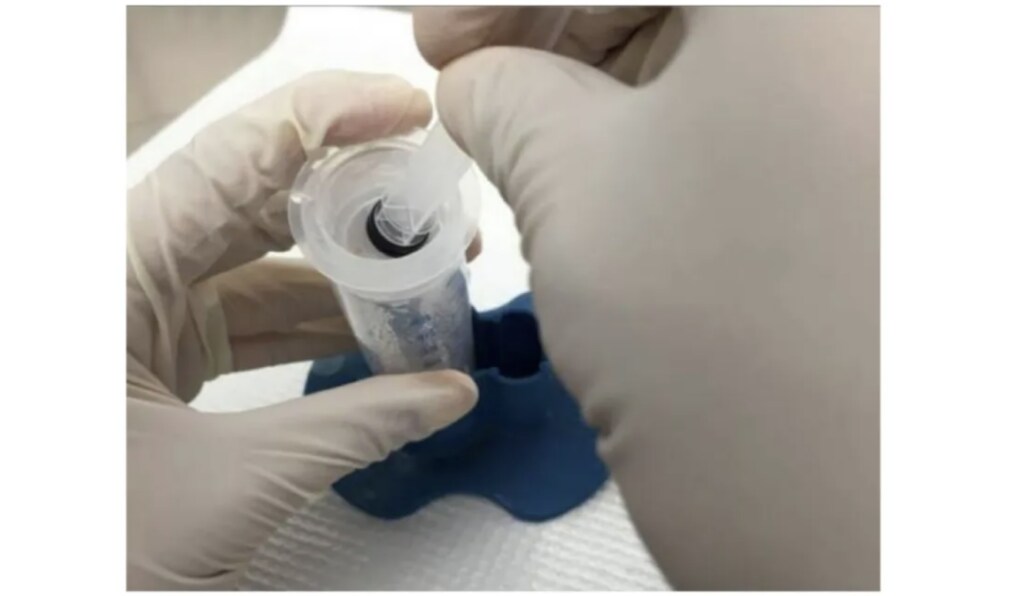
图八:进一步研磨捣碎骨髓
图九:离心后获得的骨髓细胞
13. 加入 5 mL 左右的完全培养基重悬细胞,上下吹打。可重新过筛,获取单细胞悬液。
Dr.赛友情提示:这一步红细胞还未裂解,如果需要计数建议使用AO/PI 荧光法计数有核细胞哦。推荐大家使用赛默飞的ReadyCount™ Green/Red Viability Stain (cat# A49905)搭配Countess 3FL,此试剂中AO和PI两种荧光染料的比例经过优化,可以快捷准确地反映死活细胞的数量。
14. 用适当的培养基将细胞重悬,使达到所需的细胞浓度。
15. 根据下游的应用决定是否需要裂解红细胞或者直接进行培养、分析等(红细胞裂解后也可以利用台盼蓝或AO/PI染色后进行计数哦)。
Question & Answer
Q 为什么我分离得到的骨髓细胞很少呢?
A 在剥离骨头和肌肉时,股骨的两端关节一定要完整保留,若是剪破,可能会导致细胞损失;其次,剪下的关节可进一步剪碎,股骨一定要充分冲洗直至苍白;最后收集的骨髓在过筛时可以再进行研磨。当然,如果需要尽量多的骨髓细胞,也可以再分离胫骨和肱骨内的骨髓细胞,其步骤与上述相似哦。此外,也要使用健康的小鼠进行实验。
Q 为什么我获取的骨髓细胞会出现微生物污染呢?
A 小鼠处死后,请充分为小鼠皮毛和身体灭菌。获得完整的股骨后,也可以使其浸泡与酒精中进一步消毒,实验用到的眼科剪和镊子均需要灭菌。若还是不放心,可以在培养基中添加一定的抗生素。
Q 我获得的骨髓细胞是否必须裂解红细胞呢?
A 这个问题需要根据自己的下游实验来参考文献;例如如果需要培养获取MSC, 可以不裂解直接培养;如果需要利用骨髓中单核细胞分化成为巨噬或者树突状细胞,一般需要裂红(可以使用货号为00-4333-57的裂解液,注意使用前需要过滤除菌)。有一些特殊情况,如骨髓粒细胞分离,为了不激活粒细胞,则需要用特殊的裂解方式结合密度梯度离心的方法,可以看看文献【3】哦。
Q 我该用多大周龄的小鼠分离骨髓细胞呢?获取的细胞数量在什么数量级是正常的呢?
A 一般使用成年小鼠进行实验,至少需要大于6周。如果有特殊的疾病模型,则需要进一步参考文献并结合实验摸索。文献报道,对于C57BL/6 这个品系的小鼠,收集两根股骨并裂解红细胞后,约有107-108个骨髓细胞。当然,不同周龄、品系和模型在数量上还会有差异的。
参考文献:
[1] Immune Cell Isolation from Mouse Femur Bone Marrow
[2] An improved protocol for isolation and culture of mesenchymal stem cells from mouse bone marrow
[3] Isolation, Purification and Labeling of Mouse Bone Marrow Neutrophils for Functional Studies and Adoptive Transfer Experiments


发表回复