本指南概述了质粒提取的操作流程,重点介绍了实现最佳质粒产量和纯度所需的关键材料和步骤。
从手动方法到自动化解决方案,了解如何优化质粒纯化流程,以在生物技术研究应用中获得高质量的后续结果。
目录
什么是质粒,它们在生物技术研究中的用途是什么?
质粒是一种小型、环状的DNA分子,独立于染色体DNA存在。虽然主要存在于细菌中,但其他生物体中也可能含有质粒。由于其能够自主复制,质粒成为基因操作中极为重要的工具。
质粒DNA在生物技术领域有众多应用,包括:
- 基于RNA的疫苗开发:质粒可作为模板生成用于疫苗的mRNA。通过将目标基因插入质粒并进行扩增,研究人员可以生产大量mRNA。这些mRNA随后可以被纯化,用作针对特定疾病的疫苗。
- 细胞与基因治疗:在此背景下,质粒DNA用于修复基因,以纠正遗传问题。
- 病毒载体生产:质粒用于制造病毒载体,将遗传指令递送到细胞中。
- 基因工程:质粒被用来操控生物体的遗传组成,例如培育抗虫害农作物。
- 蛋白质生产质粒可以被工程化用于生产治疗用途的蛋白质。
理解质粒克隆过程
在进行质粒纯化之前,了解其前期的标准克隆流程是非常重要的。
- 在进行质粒纯化之前,了解其前期的标准克隆流程是非常重要的。
- 选择合适的大肠杆菌菌株:不同的大肠杆菌菌株有不同的用途。常规克隆通常使用转化效率高的菌株。特殊目的可能需要经过基因工程改造、具有更高质粒稳定性的菌株。点击或轻触此处输入文本。
- 转化过程:下一步是将质粒导入感受态大肠杆菌细胞中,以实现质粒复制。点击或轻触此处输入文本。
- 菌落筛选:转化后,对菌落进行筛选,并纯化质粒以用于后续应用。
影响质粒提取产量和纯度的因素
有几个因素会影响质粒产量和纯化后质粒DNA的纯度:
- 质粒大小与设计:载体骨架的选择、插入片段的大小以及DNA插入片段对于质粒产量非常重要。
- 细菌菌株的选择不同菌株具有不同的优势,例如增强质粒稳定性或提高转化效率。
- 培养条件最佳生长条件,包括温度、pH值、氧气水平、生长时间和摇床速度,对于获得高产量的质粒至关重要。
- 抗生素使用正确的抗生素浓度有助于维持选择压力,这对于质粒保留至关重要。
- 复制起点复制起点(ori)决定了质粒的拷贝数,从而影响产量。高拷贝质粒如 pUC 能产生大量拷贝,而低拷贝质粒如 pBR322 拷贝数量较少。
质粒提取所用材料
如今,研究人员可以选择传统的手动质粒纯化流程、现成试剂盒或全自动无接触系统。
手动处理工具
培养基
可以使用几种不同类型的培养基来培养用于质粒纯化的过夜细菌培养物。
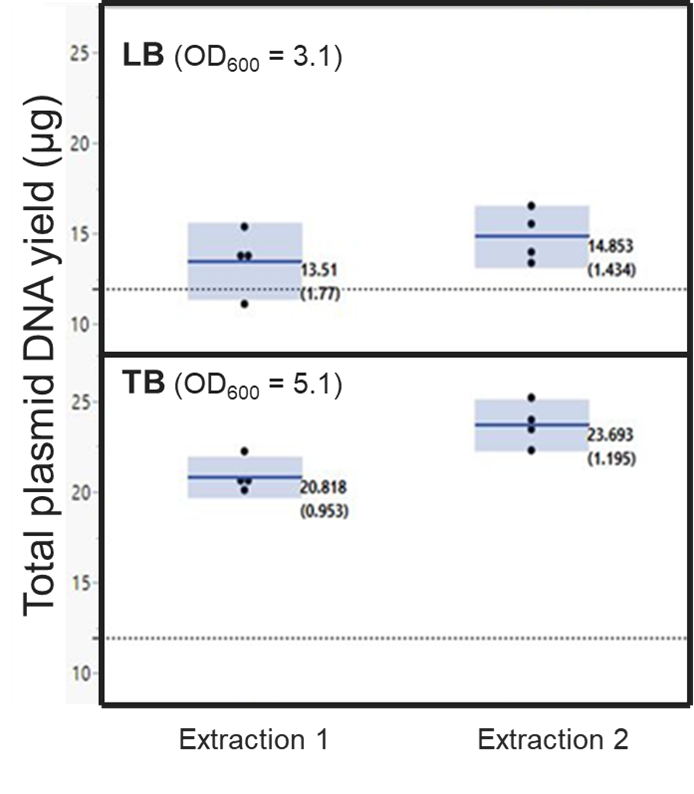
- Gibco™ 溶原性肉汤(LB)是最常用的细菌培养基。LB 培养基由蛋白胨、酵母提取物和氯化钠配制而成。根据氯化钠的浓度,LB 培养基进一步分为 LB-Miller、LB-Lennox 和低盐 LB。
- Gibco™ 特级肉汤(TB)是一种营养丰富的培养基,含有更高浓度的蛋白胨和酵母提取物,提供丰富的氮源、维生素和矿物质。TB 培养基能促进细菌生长,并支持更高密度的细菌培养,从而在较短时间内获得更多细胞。
- 2X YT 培养基™ 与典型 LB 培养基相比,其酵母提取物浓度加倍(2X),可用于促进更高密度细胞的生长和维持较长时间的生长期。
缓冲液和溶液
需要多种缓冲液和试剂来重悬细菌沉淀、裂解细菌细胞、中和溶液以沉淀DNA、洗涤杂质以及洗脱纯化后的质粒DNA。
其他实验室设备
通常需要离心机、真空过滤装置或重力流设备等进行手动操作,以纯化质粒DNA。
质粒DNA结合表面
需要硅胶或阴离子交换膜、树脂、磁珠或其他质粒DNA结合基材。
分光光度计
用于测量DNA浓度和纯度的仪器包括Thermo Scientific NanoDrop、酶标仪或其他分光光度计。
琼脂糖凝胶电泳与成像
琼脂糖凝胶电泳工具用于检测质粒DNA的完整性。
离心管
在质粒纯化过程中,会在多个步骤中使用多种可容纳不同体积试剂和缓冲液的离心管,包括微量离心管、膜柱管、澄清过滤管和收集管。所有所需的离心管都包含在质粒纯化试剂盒中。这些离心管通常由耐用且抗渗漏的材料制成,如聚丙烯或聚乙烯。这些离心管也有无内毒素版本,以满足更高纯度的需求。
通过遵循这些步骤并使用合适的材料,您可以有效地纯化质粒DNA,用于各种后续应用。
质粒提取试剂盒
传统的柱式方法为研究人员提供了从小规模质粒分离到商业规模扩大的灵活选择。手动纯化试剂盒的选择取决于实验室对起始培养体积以及后续应用所需质粒产量的需求。
以下是针对不同起始培养体积和预期质粒产量的各类柱式解决方案摘要:
小量提取(1-5mL;最高40µg)
中量提取(25-100mL;高达400µg)
大量提取(100-500mL;高达1.5mg)
大容量提取(500毫升-2.5升;最高可达5毫克)
超大容量提取(2.5-5升;最高可达15毫克)
质粒提取自动化
最新的自动化质粒分离技术相比手动方法可以帮助提高效率。
Applied Biosystems™ MagMAX™ ProHT NoSpin Miniprep 质粒分离试剂盒例如,在收获细菌细胞时,完全省去了离心步骤。该试剂盒采用双参数磁珠法,其中一组磁珠与细菌结合,另一组磁珠与质粒DNA结合,从而洗脱出更高质量的质粒DNA。
Thermo Scientific™ KingFisher™ PlasmidPro Maxi Processer是另一种工具,可以让研究人员在系统自动化几乎整个纯化流程时无需看管——从培养到转染级纯化质粒DNA只需不到75分钟,且实际操作时间仅为5分钟。
质粒提取流程中的关键步骤
质粒纯化可能是一项劳动密集且耗时的手动过程。
手动质粒分离和纯化技术通常包括以下步骤:
1. 准备过夜的细菌培养物。
此步骤用于培养细菌群体,以收获分离的质粒DNA。
- 接种:将单个细菌菌落接种到少量液体培养基中,制备起始培养物,并在37°C、225 rpm条件下培养4-8小时。使用该起始培养物接种更大量的过夜培养,用于质粒纯化。
- 生长:在最佳条件下孵育培养物(通常在37°C摇床上),直到达到所需的细胞密度(通常以OD600测量)。
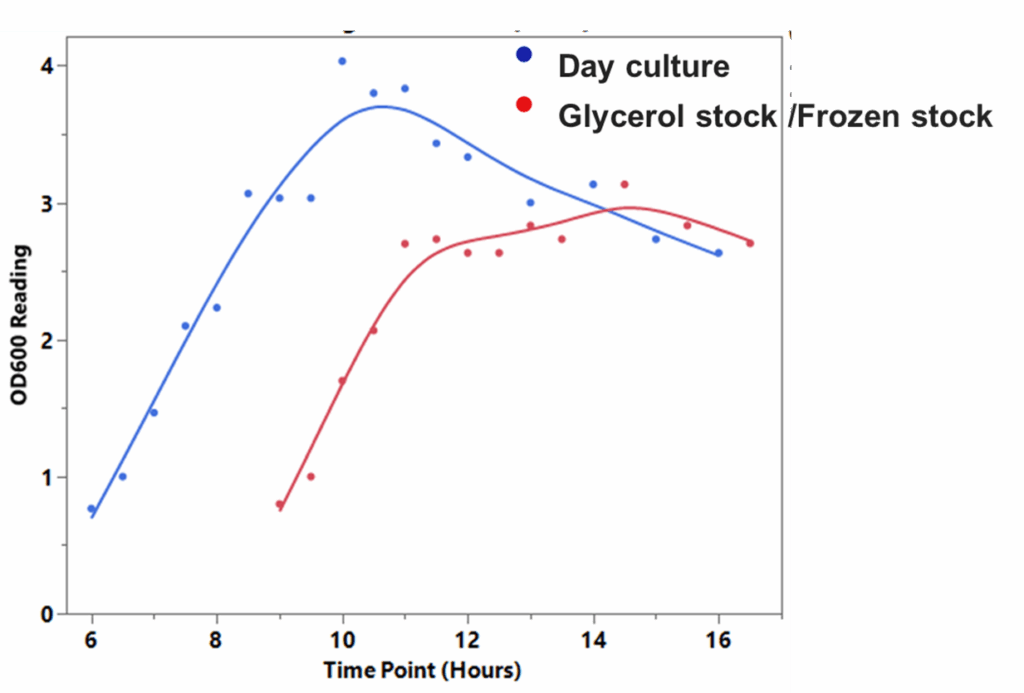
成功制备起始培养物的小贴士:使用单个菌落制备的起始培养物相比直接从冷冻菌株开始过夜细菌培养,能获得更理想的生长条件。起始培养中的细胞处于活跃生长期,即指数期,非常适合用于新培养的启动。
相比之下,冷冻菌株中的细胞由于冷冻和解冻过程带来的压力,可能存活率降低——导致生长速度变慢、滞后期延长。高拷贝质粒通常需要12-16小时生长,而低拷贝质粒可能需要20小时或更久。
2. 收获细菌细胞
此步骤将溶液中的细菌细胞收集起来,形成沉淀,以便进一步分析。
- 离心:通过离心培养物收集细菌细胞,并弃去上清液。
3. 诱导细胞裂解
此步骤的目的是溶解细菌并释放其内容物,包括遗传质粒材料,以便进一步纯化。
- 重悬:用重悬缓冲液(通常含有Tris-HCl、EDTA和RNase A)将细胞沉淀重悬。
- 裂解:加入裂解缓冲液(通常含有NaOH和SDS),以破坏细胞并释放质粒DNA。
- 中和:用中和缓冲液(通常含有醋酸钾或醋酸)中和溶液,使细胞碎片沉淀,同时保持质粒DNA在溶液中。
4. 澄清裂解液
通过离心或过滤清除裂解液,以去除沉淀杂质和其他污染物。
5. 结合质粒DNA
将澄清后的裂解液通过硅胶柱或其他DNA结合基质。质粒DNA会结合到柱子上,而杂质则流出。
6. 洗涤
用一种或多种洗涤缓冲液(通常含有乙醇和盐)洗涤柱子,以去除残留的污染物。
7. 洗脱
使用低盐缓冲液(通常含有Tris-HCl或水)将质粒DNA从柱子上洗脱下来。
8. 浓度与纯度检测
质粒纯化的最后一步是对浓度和纯度进行质量检测。
- 乙醇沉淀(可选):如有需要,可通过乙醇沉淀浓缩DNA。
- 质量控制:使用分光光度法(例如A260/A280比值)测量质粒DNA的浓度和纯度,并运行琼脂糖凝胶以检测其完整性。
更多质粒提取资源
- 学习:了解质粒纯度
- 探索与购买:质粒提取
- 自动化:Kingfisher PlasmidPro Maxi 处理器
- 探索与购买:质粒小量提取试剂盒中量提取试剂盒,以及大量提取试剂盒
- 设计:质粒纯化选择工具
- 下载电子书: 手动与自动质粒纯化解决方案的技术
##
仅供科研使用。不得用于诊断程序。
© 2025 Thermo Fisher Scientific Inc. 保留所有权利。除非另有说明,所有商标均为 Thermo Fisher Scientific 及其子公司的财产。