T细胞激活是体外获取大量T淋巴细胞基础的实验手段之一,激活和扩增获得的T细胞可广泛应用于下游CAR-T、TCR-T等研究和治疗。生理状态下,TCR(T细胞受体)会与CD3γ, ε, σ和ζ形成一个大的复合物 (图1)。发生抗原提呈时,此复合物可能发生聚集、排阻去磷酸化的分子 、募集Lck(淋巴细胞特异性蛋白酪氨酸激酶)以及释放出包埋在膜内的CD3ζ分子等,进而刺激T细胞活化和增殖。
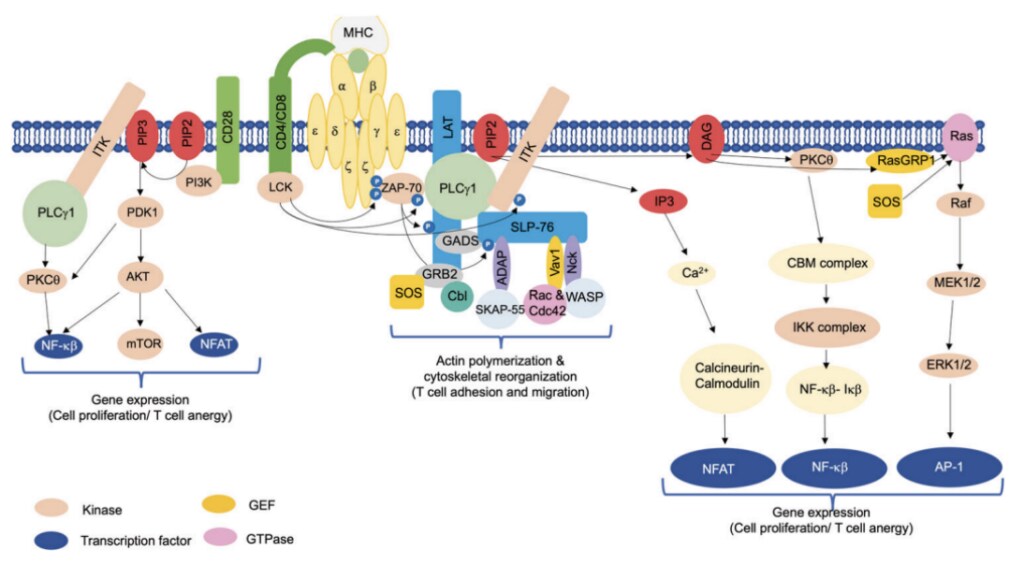
图1. T 细胞信号转导的正向调节[1]
由于CD3ε亚基在T细胞表面相对容易被抗体识别和结合,因此商品化的T细胞激活抗体大多是针对CD3ε亚基的。与抗原提呈过程类似,在体外实验中,使用CD3ε的抗体,可以有效地模拟抗原-MHC复合物与TCR的结合,从而激活下游的信号传导通路。
除了CD3构象改变引起的第一信号,T细胞的完全活化还需要另一个共刺激信号(CD28介导的第二信号)。它通常与抗原提呈细胞表面的CD80/CD86分子作用,当然也可以用CD28抗体代替CD80/CD86来诱发第二信号。
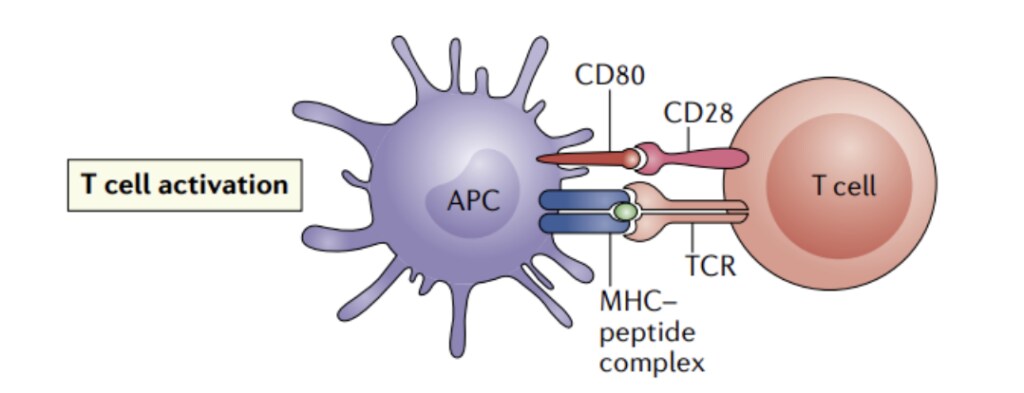
图2. T 细胞刺激[2]
CD3/CD28抗体活化T细胞操作步骤
这里以激活小鼠脾脏淋巴细胞为例
步骤 I:抗体包被96孔板
- 在无菌 PBS 中制备 5-10 µg/mL anti-CD3(货号#16-0031-82)溶液。Note:建议进行预实验,以确定其他浓度CD3抗体诱导细胞活化的功效。
- 将 50 µL 抗体溶液分配到96 孔板各孔中。对于未刺激的对照孔,添加 50 µL 无菌 PBS。
- 封口膜密封96孔板以避免液体蒸发,37°C下孵育2 h,或提前一天准备并在 4°C 下保存过夜。
- 添加细胞之前,取出50 µL抗体溶液。
- 用 200 µL 无菌 PBS 冲洗每个孔并丢弃 PBS。
- 重复上述步骤。
步骤 II:添加细胞
- 将准备好的细胞用完全培养基重悬为1-2×106/mL。Note:建议滴定细胞密度(2-3×106细胞/mL至105细胞/mL)以实现最佳活化。
- 用 PBS 清洗孔后(上述步骤 6),向每个孔中添加 100 µL 细胞悬浮液(不同条件注意设置复孔)。
- 添加CD28抗体(货号#16-0281-82),使其终浓度为 2 ug/mL。
- 放入 37°C、5% CO2 培养箱中,孵育 2-4天。Note:孵育时间需要根据实验需求进行优化,注意观察细胞状态和培养基颜色,及时更换新鲜培养基。
- 收获和处理细胞进行下游检测。
Question & Answer
Q 上述抗体刺激方案可以将T细胞扩增多少倍?
A 一般来讲,至少几十倍的扩增倍数是可以实现的。但这同时也与细胞来源、状态,以及抗体浓度和激活时间息息相关。
Q 抗原提呈的方法与用CD3/CD28抗体活化有什么区别?
A 利用抗原提呈方法活化的T细胞是某个抗原特异性的细胞,这部分细胞比例偏低,而CD3/CD28活化的T细胞是多克隆的,从而能够获得较多的T细胞。
Q 在什么时间该给T细胞进行补液或者换液呢?
A 激活过程中,需每天观察细胞是否形成克隆团。可以对细胞进行计数,如果出现培养基变黄或细胞密度过高的情况,可吹散细胞克隆团后调整细胞密度至0.5-1×106/ml,离心重悬在新鲜培养基中。
Q 如果我需要观察T细胞增殖能力,有哪些方案呢?
A 可以采用细胞计数的方法,也可以利用染料稀释法观察T细胞的增殖代数,推荐使用CellTrace细胞增殖检测试剂(例如Celltrace CFSE,货号C34554),此外利用Click-it EdU的方法也可以检测不同刺激条件下T细胞的增殖能力。
Q CD3/CD28磁珠激活与CD3/CD28抗体激活T细胞有什么区别?
A 磁珠提供了多价交联信号,通常激活强度较高且持续时间较长,能够更有效地模拟天然APC的作用,但价格较高,常用于需要高效激活T细胞的实验;抗体激活的操作相对简单,激活强度和持续时间可能相对较弱,适用于一般的T细胞激活实验。
其他可参考的T细胞刺激活化方法[3]
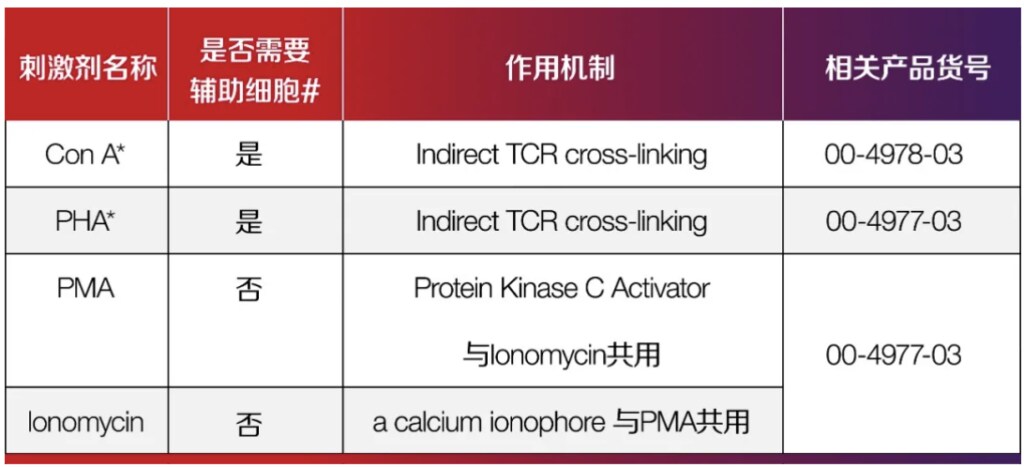
*ConA和PHA 作用机制类似,两者可以结合细胞膜蛋白上的糖基基团,诱发T细胞受体的交联,从而激活T细胞。
*辅助细胞:与APC细胞功能类似,为T细胞激活提供共刺激分子或者Fc受体(可提供抗体结合位点)。细胞来源可以是删除或未删除T细胞的其他免疫细胞组分。为避免辅助细胞的背景增殖,可以用细胞色素C或者γ射线进行处理。
参考文献:
[1] K Shah, K., Al-Haidari, A., Sun, J., & Kazi, J. U. (2021). T cell receptor (TCR) signaling in health and disease. Signal transduction and targeted therapy, 6(1), 412. doi: 10.1038/s41392-021-00823-w.
[2] Cappell, K. M., & Kochenderfer, J. N. (2021). A comparison of chimeric antigen receptors containing CD28 versus 4-1BB costimulatory domains. Nature reviews Clinical oncology, 18(11), 715-727. doi: 10.1038/s41571-021-00530-z
[3] Kruisbeek, A. M., Shevach, E., & Thornton, A. M. (2004). Proliferative Assays for T Cell Function. Current Protocols in Immunology. doi:10.1002/0471142735.im0312s60


发表回复