1. 高质量RNA
降解或不纯的RNA会限制逆转录反应的效率并降低产量。
降解或不纯的RNA会限制逆转录反应的效率并降低产量。RNA应从新鲜组织中制备,或使用如Invitrogen™ RNAlater®稳定液处理的组织中制备。因此,部分RNA降解是可以容忍的。如果无法使用完全完整的RNA,请设计引物使其与目标基因的内部区域结合。请注意,对于真正的定量RT-PCR,部分降解的RNA可能无法准确反映基因表达情况。
2. 良好的引物和探针设计
为了最有效地设计实时PCR用的引物和探针组合,我们强烈建议使用引物设计软件。大多数引物设计程序都包含可调参数,以实现最佳引物和探针设计。这些参数考虑了引物/探针Tm、互补性、二级结构,以及扩增片段大小等其他重要因素。同时建议限制相同核苷酸连续出现的数量。在为真核生物目标设计扩增片段时,应选择跨越目标mRNA至少一个外显子-外显子连接处的PCR引物,以防止来自污染基因组DNA的目标扩增。
如果你想完全避免设计的工作,可以选择预先设计好的 Applied Biosystems™ TaqMan® 检测试剂。每个检测试剂都包含所需的一切——目标引物和优化的序列特异性探针——无需额外设计、优化或冗长的熔解曲线分析。
3. 使用 Master Mix(主混合液)
主混合液将所有 qPCR 试剂混合在一起,有助于减少样品间和孔间的差异,并提高重复性。为了进一步减少孔间差异,请使用含有参考染料(如 ROX)的主混合液。请参考这个实用的选择指南来为你的实验选择合适的主混合液(你甚至可以获得一个免费样品)。
4. 避免交叉污染
PCR区域内的所有表面都应定期去污,以防止交叉污染。建议使用DNA去污溶液,如Invitrogen™ DNAzap™ PCR DNA降解溶液,该溶液能够破坏DNA。应运行一个“无模板对照”(NTC),以排除试剂和表面的交叉污染。NTC包含所有RT-PCR试剂除了
核酸模板。通常,DNA或RNA只需用无核酸酶水替代。在NTC中不应合成任何产物;如果扩增出产物,则说明一个或多个RT-PCR试剂被扩增子污染了。
如需了解更多信息,请阅读这篇关于在qPCR实验中避免污染的良好实验室规范的文章。
5. 使用“无逆转录酶”对照(No RT Control)
乎不可能完全消除RNA制备中的基因组DNA。因此,在qPCR实验中加入一个减去逆转录酶对照(“无扩增对照”或NAC)非常重要。通常,NAC是一个模拟逆转录反应,包含所有试剂,除了逆转录酶。如果在NAC中观察到产物,这很可能表明样品中存在污染的DNA。
一个更简单的解决方案是使用跨越外显子-外显子连接位点的检测方法。通过利用这种只存在于RNA(或cDNA)中的独特序列,就不会检测到基因组DNA。在查找预设计TaqMan检测试剂时,您可以筛选那些不会检测基因组DNA的试剂。
6. 使用合适的归一化对照
通过在实验中加入一个不变的内源性对照,可以提高任何qPCR实验的可靠性,以校正样品间的差异。一个好的对照其表达水平在所分析样品之间不应有变化。18S rRNA常被用作对照,因为其表达水平比其他传统内参如β-肌动蛋白或GAPDH更为稳定。如需了解更多关于选择内源性对照的信息,请下载此份应用说明。

7. 使用 SYBR® Green 进行解离(熔解)曲线分析
理想情况下,实验样品在扩增子熔解温度处应产生一个尖锐的峰值(一阶导数图),而 NAC 和 NTC 不会产生显著的荧光信号。该结果表明产物具有特异性,并且SYBR Green荧光是目标产物积累的直接测量指标。如果解离曲线显示一系列峰值,则说明对特异性和非特异性反应产物的区分不够。为了获得有意义的数据,需要进行优化。
使用 TaqMan 检测试剂避免优化和熔解曲线分析的必要性。预设计、基于探针的 TaqMan 检测试剂 不仅为您进行了优化,还提供了性能保证。
8. 正确设置基线和阈值
为了获得准确的 Ct 值,基线需要比最丰富样品的 Ct 值提前两个循环设置。要使实时 PCR 数据有意义,阈值应在产物处于指数增长阶段时设定。新的 Applied Biosystems 仪器和 Thermo Fisher Connect(云端)都具备自动设置基线和阈值的算法。一种名为相对阈值或 C 的新算法RT可以用于确定Cq。请查阅应用说明,CRT,一种用于qPCR数据分析的相对阈值方法…,以获取更多信息。
快速回顾:相对阈值(Crt)方法。
下图和步骤描述了如何计算Crt。扩增曲线为蓝色;反应效率曲线模型为红色;左侧y轴对应蓝色扩增曲线,右侧y轴对应红色曲线。Crt的确定分为四个步骤:
使用预设的内部参考效率水平(粉色虚线)来识别反应效率曲线(模型)达到特定数值时的小数周期(Ce)。
- 使用预设的内部参考效率水平(粉色虚线)来确定反应效率曲线(模型)达到特定值时的分数周期(Ce)。
- 荧光水平(Fe)对应于扩增曲线上的分数循环Ce。
- 相对荧光阈值(浅蓝色虚线)是根据Fe的特定百分比(%Fe)计算得出的曲线特异性阈值。
- Crt被计算为扩增曲线与相对荧光阈值交叉时的分数循环。
9. 确认反应效率
反应的效率(Eff)可通过以下公式计算:
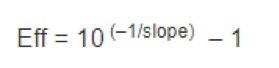
PCR的效率应为90–110%(3.6 > 斜率 > 3.1)。多种变量会影响PCR的效率,包括扩增子长度、二级结构和引物设计等。虽然可以获得落在该效率范围之外的有效数据,但仍建议进一步优化qPCR,或设计替代扩增子。
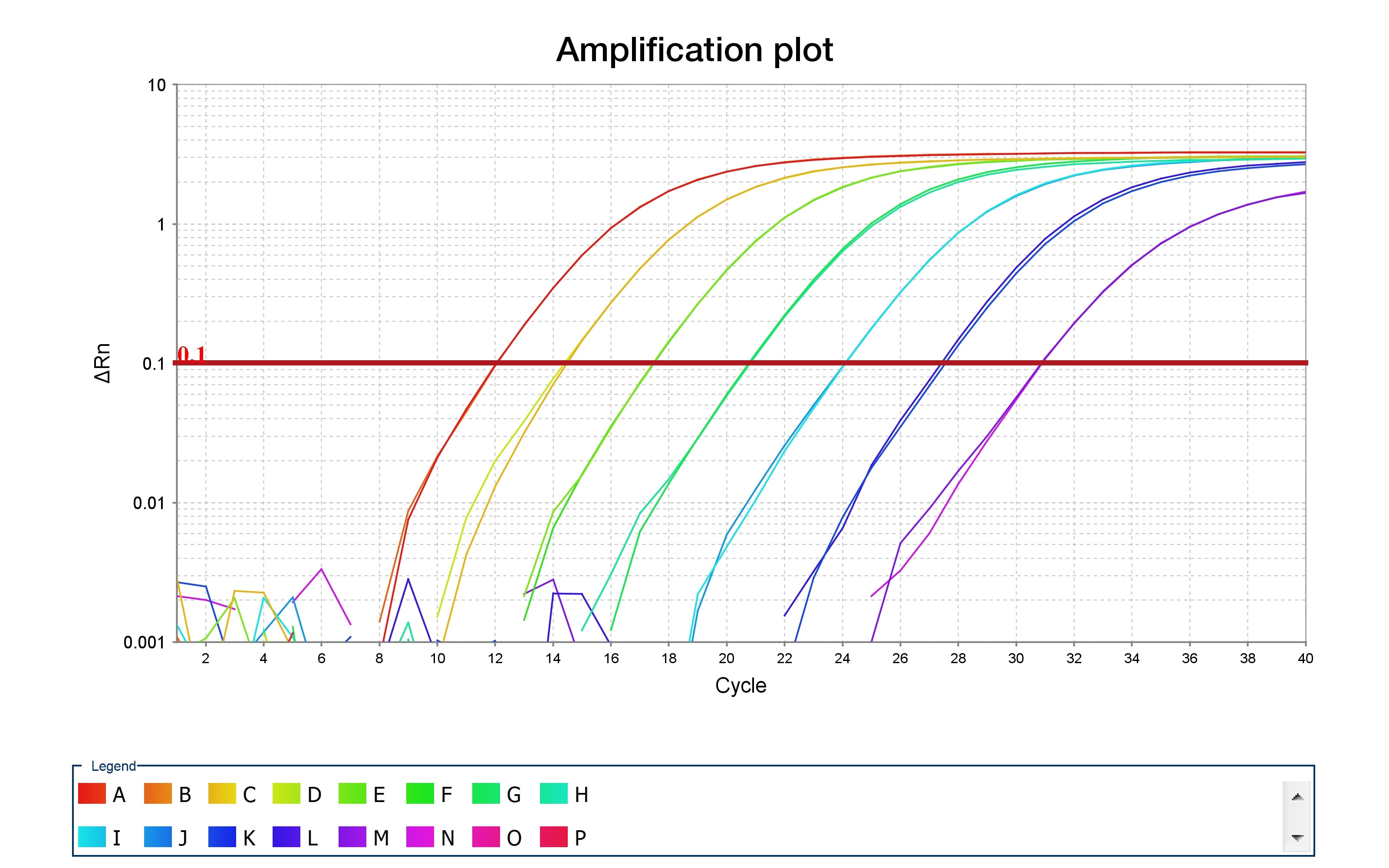
10. 使用适当范围的标准曲线
对于RNA定量(绝对或相对定量)研究中的每个基因,或用于比较定量(delta-delta-Ct)中验证反应效率,应分别制备标准曲线。标准曲线应覆盖目标预期丰度以上和以下的范围。还可以包括其他输入量,如高于和低于检测限的最小和最大RNA用量,以帮助区分特异性产物和非特异性产物。
仅供科研使用。不用于诊断程序。





发表回复