想象一下,一枚能够精确锁定癌细胞而相对不伤害健康细胞的制导导弹。这正是抗体药物偶联物(ADC)的基本理念。这些令人着迷的分子正在成为医学领域的重要力量,尤其是在抗击癌症方面,而且这个领域正在迅速发展。
ADC市场正处于蓬勃发展阶段。曾经只是一个小众领域,如今已成为数十亿美元的产业,并且预计还将持续增长。原因是什么?因为ADC在治疗各种癌症方面展现出了真正的希望,从乳腺癌、淋巴瘤到白血病。能够将强效化疗药物直接输送到癌细胞内部,最大限度减少传统化疗带来的严重副作用,这无疑是一次重大突破。
目录
什么是抗体药物偶联物(ADC)?
抗体-药物偶联物(ADC)是一种靶向癌症治疗方法,将单克隆抗体的特异性与细胞毒性药物的高效杀伤力相结合。这种方法能够将化疗药物直接输送到癌细胞,从而最大程度减少对健康组织的损伤。
类比科学:ADC作为针对疾病靶点的“智能炸弹”
从科学角度来看,ADC是生物治疗领域中多种理念巧妙结合的产物。
首先是抗体,它就像一个定位装置,能够特异性识别癌细胞或其他疾病靶点上的抗原标记。然后是作为“弹头”的强效药物,用于杀死这些细胞。两者之间至关重要的分子连接被称为连接子。
科学家们不断致力于研发更具针对性的抗体、开发更强大且更有针对性的药物,并设计出在血液中稳定但能在到达肿瘤后释放有效载荷的连接子。目前我们还看到了一些新方法,比如使用能够同时识别癌细胞多个标记的双特异性抗体,或者携带不同类型药物(如可增强患者自身免疫系统功能的药物)的抗体。
ADC治疗组成部分
从结构上看,ADC由三部分组成:一种能与肿瘤相关抗原结合的单克隆抗体、一种细胞毒性有效载荷,以及将二者连接起来的化学连接子。该抗体能够靶向在癌细胞上高表达的抗原,实现选择性递送。
单克隆抗体(mAb)
单克隆抗体作为靶向部分,被设计用于识别并结合那些在肿瘤细胞上高表达、而在正常组织上极少存在的特定抗原。这种特异性促进了细胞毒性载荷对恶性细胞的选择性递送,提高了治疗效果,同时减少了全身毒性。
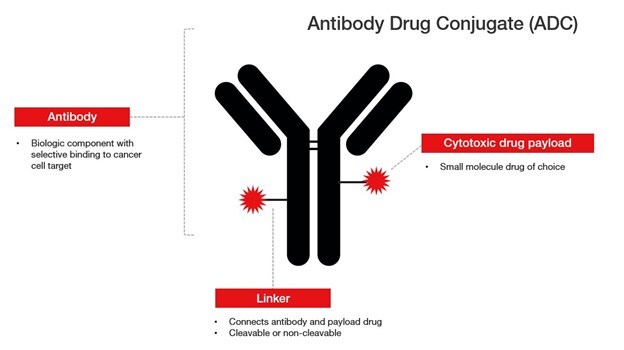
连接子
连接子是一种化学桥梁,将单克隆抗体与细胞毒性载荷连接起来。它必须在血液中保持稳定,以防止药物过早释放,同时又能在目标细胞内被切割,从而确保有效递送载荷。连接子分为可切割型和不可切割型。可切割型连接子利用细胞内环境
——如酸性pH值或特定酶(如组织蛋白酶)——来释放载荷,而不可切割型连接子则依赖于抗体在溶酶体中的完全降解以释放活性药物。
细胞毒性有效载荷
细胞毒性载荷是一种高效的小分子药物,旨在被癌细胞内吞后杀死癌细胞。常见的载荷包括微管抑制剂(如单甲基奥瑞司他汀E)和DNA损伤剂(如卡利奇霉素)。由于其高毒性,这些药物不适合全身给药,但通过ADC选择性递送时效果显著。
双载荷抗体药物偶联物(ADC)
ADC技术的新兴进展之一是双载荷ADC的开发,即在一个偶联物中包含两种不同的细胞毒性药物。这一策略旨在通过同时靶向多条细胞通路,解决肿瘤异质性和耐药问题。双载荷ADC可以设计为递送具有互补作用机制的药物,有望增强抗肿瘤活性并克服单一药物治疗的耐药问题。
抗体药物偶联物(ADC)是如何发挥作用的?
ADC与其目标抗原结合后,通过受体介导的内吞作用进入癌细胞。该复合物被运输至溶酶体,在此处连接子被切割,释放出细胞毒性药物。
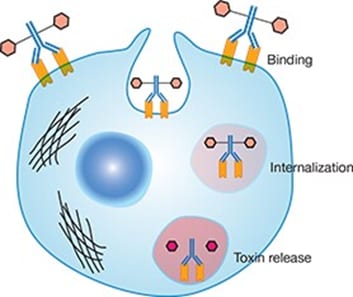
在溶酶体内,连接子在控制细胞毒载荷释放方面起着关键作用。连接子设计为在循环中稳定,但能在细胞内环境中被切割,常常利用酸性pH或特定溶酶体酶。例如,对半胱天冬酶B敏感的肽基连接子被广泛采用,以确保细胞毒剂主要在目标细胞的溶酶体中释放。
一旦释放,细胞毒载荷会破坏关键的细胞过程,如DNA复制或微管功能,导致癌细胞死亡。一些ADC还具有“旁观者效应”,即释放出的药物可扩散到邻近的肿瘤细胞,包括那些缺乏目标抗原的细胞。这种旁观者现象对于治疗异质性肿瘤尤为有益,因为并非所有细胞都均匀表达目标抗原。
ADC临床成功依赖于每个组成部分的精心优化——抗体特异性、连接子的稳定性和可切割性,以及载荷效力。连接子技术的发展,如双酶可切割连接子,进一步提升了ADC的特异性和疗效。
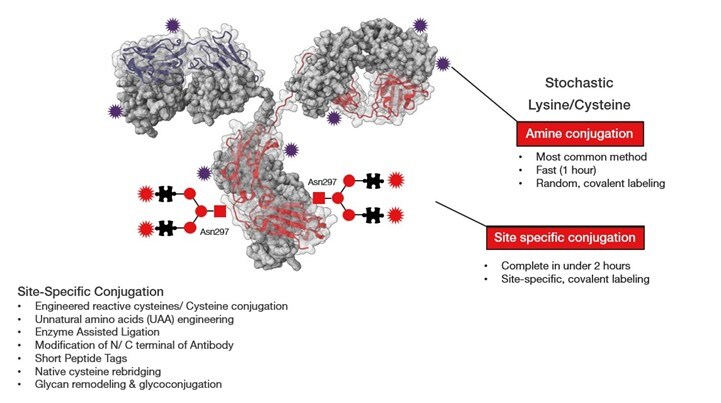
作用机制一览
- 靶点结合:ADC中的单克隆抗体组分能够特异性地结合表达于癌细胞表面的抗原。
- 内化:在结合后,ADC-抗原复合物被通过内吞作用进入癌细胞。
- 药物释放:在细胞内部,将连接抗体与细胞毒性药物的连接子切断,通常发生在溶酶体区室内,从而释放活性药物。
- 细胞死亡:释放出的细胞毒性剂干扰关键的细胞过程,如DNA复制或微管功能,导致癌细胞死亡。
ADC开发与生产工具
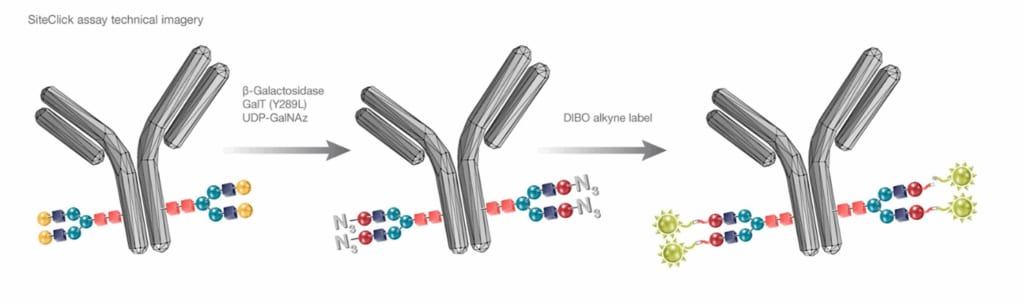
在赛默飞世尔科技,我们提供广泛的工具和技术,帮助研究人员和制造商更高效、更安全地开发和生产ADC。这包括从细胞培养系统如Gibco™ ExpiCHO™ 表达系统用于抗体生产,到抗体偶联工具如Invitrogen™ SiteClick™ 抗体标记试剂盒或我们的定制重组抗体服务。
优化ADC工作流程的工具
- 基因合成与高通量抗体表达:GeneArt HTP抗体表达服务一个半自动化、高通量的平台,可实现从瞬时转染的哺乳动物细胞中可重复且快速地生产抗体。
- 表达与纯化:ExpiCHO表达系统用于实现抗体及非抗体蛋白瞬时表达产量达1-3克/升;Nalgene 5升斜口烧瓶
- 抗体标记:SiteClick或LysoLight标记试剂盒通过荧光显微镜、流式细胞仪或高内涵成像平台,实现对溶酶体内吞抗体的特异性和敏感性检测
- 成像与高内涵分析:EVOS M7000 成像系统,CellInsight CX7 LZR Pro 高内涵筛选平台
FDA批准的ADC药物
截至2025年5月,FDA已批准15种ADC药物用于临床应用。还有一百多种ADC候选药物正在临床管线中进行评估。
| Drug | Approval year | Payload | Target | Disease Indication |
|---|---|---|---|---|
| Gemtuzumab Ozogamicin (Mylotarg) | 2000*, 2017 | Calicheamicin | CD33 | Acute myelogenous leukemia (AML) |
| Brentuximab Vedotin (Adcetris) | 2011 | MMAE | CD30 | Hodgkin lymphoma (HL), anaplastic large cell lymphoma (ALCL) |
| Trastuzumab Emtansine (Kadcyla) | 2013 | DM1 | HER2 | Breast cancer |
| Inotuzumab Ozogamicin (Besponsa) | 2017 | Calicheamicin | CD22 | Acute lymphoblastic leukemia (ALL) |
| Moxetumomab Pasudotox (Lumoxiti) | 2018* | PE38 | CD22 | Hairy cell leukemia (HCL) |
| Polatuzumab Vedotin (Polivy) | 2019 | MMAE | CD79b | Diffuse large b-cell lymphoma (DLBCL) |
| Enfortumab Vedotin (Padcev) | 2019 | MMAE | Nectin-4 | Urothelial (bladder) cancer |
| Trastuzumab Deruxtecan (Enhertu) | 2019 | DXD | HER2 | Breast cancer |
| Belantamab mafodotin-blmf (Blenrep) | 2020* | MMAF | BCMA | Multiple myeloma |
| Sacituzumab Govitecan (Trodelvy) | 2020 | SN-38 | TROP2 | Breast cancer, urothelial (bladder) cancer |
| Disitamab Vedotin (Aidixi) | 2021 | MMAE | HER2 | Gastric cancer, urothelial (bladder) cancer |
| Loncastuximab Tesirine (Zynlonta) | 2021 | PBD SG3199 | CD19 | Diffuse large b-cell lymphoma (DLBCL) |
| Tisotumab Vedotin (Tivdak) | 2021 | MMAE | TF | Cervical cancer |
| Mirvetuximab Soravtansine (Elahere) | 2022 | DM4 | FRα | Ovarian cancer |
| Datopotamab Deruxtecan (Datroway) | 2025 | DXD | TROP-2 | HR+/HER2– breast cancer |
| Telisotuzumab vedotin (Emrelis) | 2025 | MMAE | c-Met | non-small cell lung cancer (NSCLC) |
*产品已撤回或停止上市
2025年的监管环境
美国食品药品监督管理局(FDA)已将ADC归类为组合产品,包括生物制品(抗体)和药物(细胞毒性载荷)。这种分类要求遵守与生物制品和小分子药物相关的监管要求,影响制造流程、质量控制以及审批路径。
2025年4月,FDA宣布了一项战略举措逐步淘汰传统动物实验在药物开发中的应用,包括ADC的开发。该机构鼓励采用新方法学(NAMs),如基于人工智能的模型和实验室构建的人类类器官结构,以提升药物安全性评估并减少对动物模型的依赖。
FDA有时也为ADC疗法提供加速审批途径。例如,在2025年5月,该机构授予了加速批准艾美瑞利(telisotuzumab vedotin)用于治疗曾接受过治疗的、表现出高c-Met蛋白过度表达的非鳞状非小细胞肺癌(NSCLC)成人患者。
ADCs的未来发展方向
展望未来,抗体药物偶联物(ADC)领域令人非常振奋。我们有望看到更加精准的靶向策略,例如使用由抗体片段或细胞表面受体结合基团衍生出的更小型靶向分子,或针对癌细胞上的新型标志物。科学家们还在研发“更智能”的连接子,使其能在肿瘤环境中更特异性地释放有效载荷。联合疗法,即ADC与其他癌症治疗方法如免疫疗法共同使用,也展现出巨大前景。除了癌症之外,研究人员还在探索ADC用于治疗其他疾病的潜力,如自身免疫性疾病甚至感染。
简而言之,抗体药物偶联物代表了一种强大且不断发展的靶向治疗方式。虽然其开发和生产过程中存在挑战,但科学进步以及提供创新解决方案企业的努力正在为未来铺路,让这些“智能炸弹”能够为各种疾病提供更有效且毒性更低的治疗方案。
更多资源
- 手册:抗体药物偶联物筛选 及特性分析
- 工具: 抗体内吞和降解分析用于ADC发现
- 工具: 用于ADC筛选和表征的改进标记工具
- 海报: 利用点击化学实现抗体基构建模块化、可控组装
- 应用说明: 抗体-药物偶联物开发:从抗体生产到表征
##
© 2025 Thermo Fisher Scientific Inc. 保留所有权利。所有商标均属于Thermo Fisher Scientific及其子公司,除非另有说明。另有说明。
仅供科研使用。不得用于诊断程序。




发表回复