Search
精准治疗——治疗新靶标:突破新药研发瓶颈

一个平台研究蛋白质、后修饰、代谢物,筛选免疫反应、
信号通路中的关键分子,发现药物治疗新靶标
绝大多数的药物治疗靶标都是蛋白质,例如肿瘤靶向药物多为激酶抑制剂,作用靶标为肿瘤信号通路中的 激酶;抗体药物和细胞治疗多针对肿瘤细胞表面受体/ 抗原,介导免疫反应和细胞毒性(图1)。研究表明, 人体中全部的药物靶点蛋白超过1 万种,而目前发现的靶点仅有500种左右。疾病的精准治疗亟待大量全 新治疗靶标的发现与使用。
基于Orbitrap 超高分辨质谱的蛋白质组分析是高通量发现潜在治疗靶标的利器。2015年启动的人类免 疫肽组学计划(HIPP, https://www.hupo.org/Human-Immuno-Peptidome-Project),即致力于使用蛋白质 组学手段,收集并测定人细胞表面MHC-I与MHC-II (或称HLA)呈现的所有肽段序列,更透彻地理解免疫系 统,指导并加快下一代疫苗的更透彻地理解免疫系统,指导并加快下一代疫苗的案的开发(图2)。
基于Orbitrap 超高分辨质谱的蛋白质组分析可以用于疫苗开发、治疗靶标发现、药物作用靶点研究等,突破新药研发创制瓶颈,让精准治疗更精准。
1 探索新冠新疗法,蛋白质组学在行动
法兰克福大学医学病毒学研究所 和歌德大学医学院团队发表最新 研究中,建立感染SARS-CoV-2 的Caco-212 细胞模型, 运用一 种新颖的多重增强蛋白质动力 学(multiplexed enhanced protein dynamicsme, mePROD) 方法进行 蛋白质组学分析,能够在高时间 分辨率下确定转录组和蛋白质组 的变化,加速确证病毒致病性相 关的生物途径以及寻找潜在的药 物靶标。

 测试核苷酸合成抑制剂对细胞中SARS-CoV-2 复制的影响,高达10 μM 的布雷奎纳,并不具有抗病毒的作用。相比之下,低浓度下的利巴韦林即可抑制SARS-CoV-2 复制,这表明利巴韦林是可以进行进一步检测的候选药物。
测试核苷酸合成抑制剂对细胞中SARS-CoV-2 复制的影响,高达10 μM 的布雷奎纳,并不具有抗病毒的作用。相比之下,低浓度下的利巴韦林即可抑制SARS-CoV-2 复制,这表明利巴韦林是可以进行进一步检测的候选药物。
此外,与蛋白质折叠相关的蛋白变化与病毒蛋白质较为一致,特别是AAA 家族的六聚体ATPase 酶 - p97。测试p97 的小分子抑制剂NMS–873 对SARS-CoV-2 复制的影响。研究表明,NMS–873 在低纳摩尔浓度下即可完全抑制SARS-CoV–2。
2 治疗方案
未来,蛋白质组检测将越来越多地应用于肿瘤免疫治疗方案的选择。通过蛋白质组学方法直接检测活检样本的肿瘤微环境,鉴定肿瘤细胞表面蛋白,根据表面抗原 / 免疫检查点的表达与呈现情况,个性化地制定治疗方案。
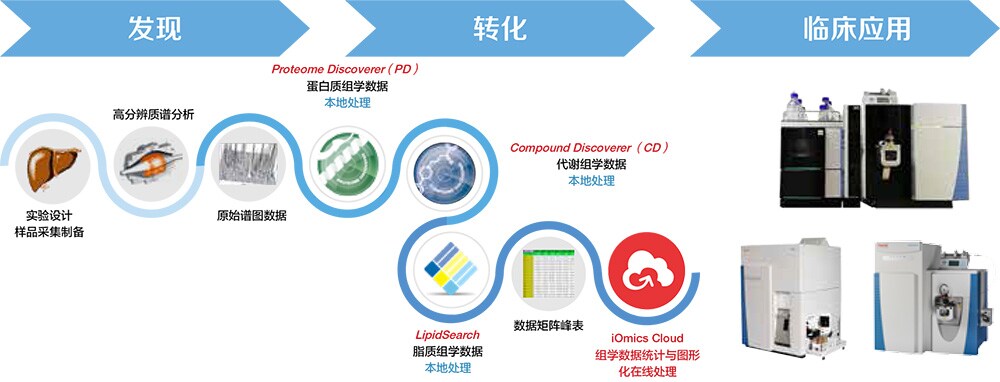
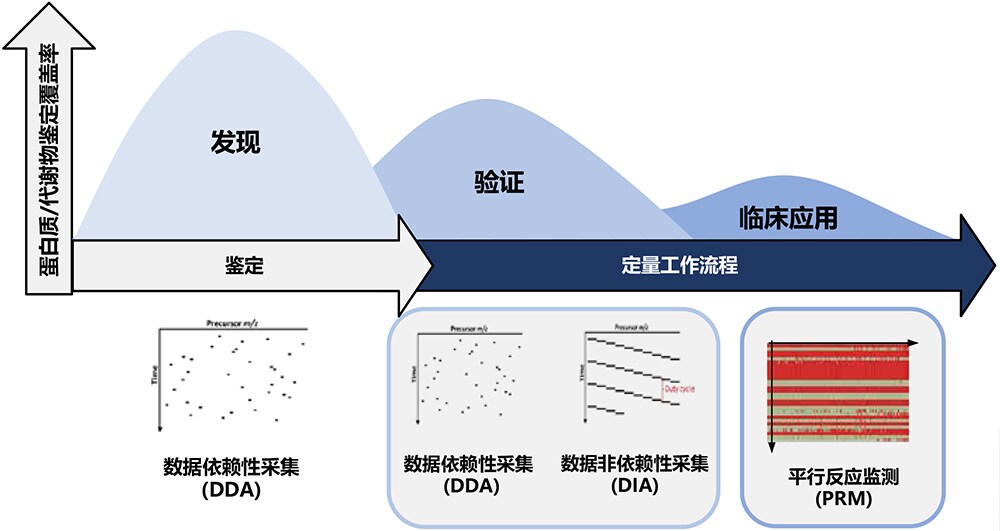
赛默飞Orbitrap 技术
助力疾病标志物发现到临床应用全过程

绝大多数的药物治疗靶标都是蛋白质。研究表明,人体中全部的药物靶点蛋白超过1万种,而目前发现的靶点仅有500种左右。疾病的精准治疗亟待大量全新治疗靶标的发现与使用。Nature Reviews Cancer, 2012, 12: 553
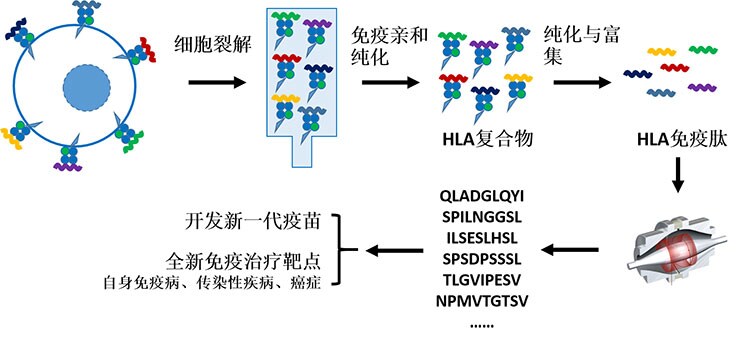
2015年启动的人类免疫肽组学计划(HIPP),即致力于使用蛋白质组学手段,收集并测定人细胞表面MHC-I与MHC-II(或称HLA)呈现的所有肽段序列,更透彻地理解免疫系统,指导并加快下一代疫苗的开发和自身免疫病、传染性疾病、癌症免疫治疗方案的开发。
基于免疫肽组学开发新一代疫苗与免疫治疗靶标。
参考文献
- Mass Spectrometry of Human Leukocyte Antigen Class I Peptidomes Reveals Strong Effects of Protein Abundance and Turnover on Antigen Presentation (Mol Cell Proteomics, 2015, 14: 658)(人免疫肽组学研究)
- The antigenic landscape of multiple myeloma: mass spectrometry (re)defines targets for T-cell–based immunotherapy (Blood, 2015, 126: 1203)(T细胞治疗潜在靶标发现)
- Adenanthin targets peroxiredoxin I and II to induce differentiation of leukemic cells (Nat Chem Biol, 2012, 8: 486)(腺花素作用靶点研究)

疫苗开发
通过蛋白质组学鉴定细胞表面呈现的外源性多肽序列或肿瘤特异性多肽序列,作为潜在的传染性疾病疫苗或肿瘤疫苗。Nature Reviews Cancer, 2002, 2: 514
治疗靶标发现
通过蛋白质组学发现并确定疾病特异的信号通路蛋白、细胞表面受体/抗原,作为潜在的治疗靶标,开发新药或新的治疗方法。如,多发性骨髓瘤全新治疗靶标的发现(Blood, 2015, 126: 1203)。
药物靶点研究
通过蛋白质组学发现并确定药物作用的靶点蛋白,研究药物机理,为进一步新药研发创制奠定基础。腺花素作用靶点的发现(Nat Chem Biol, 2012, 8: 486)。

个性化治疗
未来,蛋白质组检测将越来越多地应用于肿瘤免疫治疗方案的选择。通过蛋白质组学方法直接检测活检样本的肿瘤微环境,鉴定肿瘤细胞表面蛋白,根据表面抗原/免疫检查点的表达与呈现情况,个性化地制定治疗方案。
精确治疗典型应用
人类免疫肽组学计划——新一代疫苗与免疫治疗开发
2015年启动的人类免疫肽组学计划(HIPP),即致力于使用蛋白质组学手段,收集并测定人细胞表面MHC-I与MHC-II(或称HLA)呈现的所有肽段序列,更透彻地理解免疫系统,指导并加快下一代疫苗的开发和自身免疫病、传染性疾病、癌症免疫治疗方案的开发。基于Orbitrap超高分辨质谱的蛋白质组分析是高通量发现潜在治疗靶标的利器
发现多发性骨髓瘤全新治疗靶标
通过蛋白质组学发现并确定疾病特异的信号通路蛋白、细胞表面受体/抗原,作为潜在的治疗靶标,开发新药或新的治疗方法。如,对比多发性骨髓瘤患者与健康人细胞表面的HLA蛋白/多肽,发现了多种肿瘤特异性HLA蛋白/多肽,并成功验证了6个多肽会使T细胞响应,是潜在的T细胞免疫治疗的候选抗原。


