Search
Thermo Scientific™
沙保氏葡萄糖琼脂,干粉
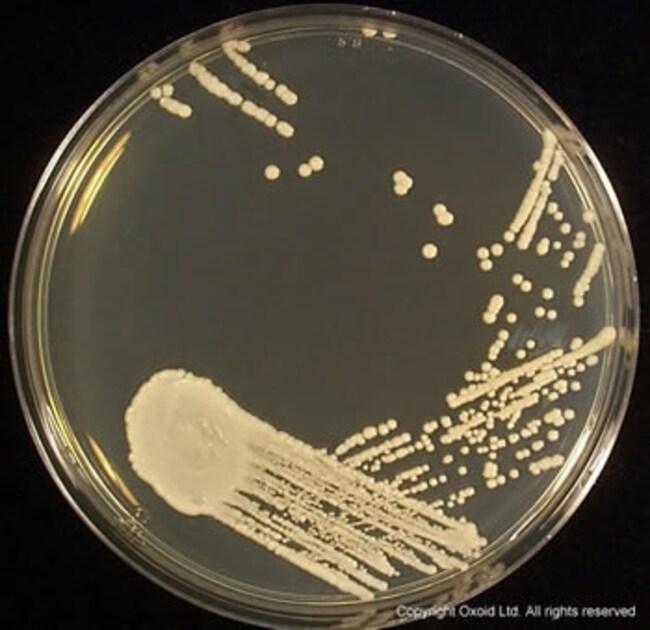
酸性 Thermo Scientific™ Oxoid™ 沙保氏葡萄糖琼脂可用于鉴定癣菌和其他真菌及酵母。
| 货号 | 数量 |
|---|---|
| CM0041R | 2.5 kg |
| CM0041T | 5 kg |
| CM0041K | 25 kg |
| CM0041B | 500 g |
货号 CM0041R
价格(CNY)
-
数量:
2.5 kg
酸性 Thermo Scientific™ Oxoid™ 沙氏葡萄糖琼脂可用于鉴定临床标本和环境样品中的癣菌和其他真菌及酵母。低 pH 值支持混合样品中的真菌生长,同时抑制细菌生长。真菌会保持它们的典型培养外观,因此,可以根据标准的宏观特性容易地鉴定。
Oxoid 沙保氏葡萄糖琼脂是一种改良沙保氏琼脂,可用于培养和区分真菌 (Carlier1)。该培养基通常与抗生素一起使用,用于将致病真菌从含有大量其他真菌或细菌的材料中分离出来。
Georg 等人2在无菌条件下将 0.5g 环己酰亚胺、20,000 单位的青霉素和 40,000 单位的链霉素加入到每升经高温高压灭菌并冷却的培养基中。新型隐球菌、烟曲霉和波伊德氏霉杆真菌对环己酰亚胺敏感;牛放线菌和星形诺卡菌对青霉素和链霉素敏感。或者,可在高压灭菌前添加 0.4g 氯霉素和 0.05g 环己酰亚胺到每升再水化培养基中 (Ajello3)。同样的微生物对这一新的组合敏感(见皮肤真菌选择添加剂 SR0075E)。
Williams Smith & Jones4 采用 Oxoid 沙保氏葡萄糖琼脂,每升培养基含 20,000 单位青霉素和 0.04g 新霉素,用于猪消化道内的酵母菌计数。Hantschke5 使用粘菌素、新生霉素和环己酰亚胺分离白色念珠菌。Dolan6 使用庆大霉素、氯霉素和环己酰亚胺用于致病真菌的选择性分离。
Oxoid 沙氏葡萄糖琼脂也可以用作 Pagano-Levin 培养基的基质7,用于分离白色念珠菌。将 0.1g 氯化三苯基四氮唑(作为过滤灭菌溶液)添加到每升经高温高压灭菌然后冷却到 55°C 的熔融培养基中。通常通过加入抗生素将该培养基制成能抑制大多数非致病真菌和细菌的培养基,如上所述。在 25°C 下培养 3 天后,白色念珠菌菌落为未着色或浅粉色,而其他念珠菌属和其他真菌形成较深的粉色或红色菌落。该试验足以用于筛查目的,但其他的诊断标准也应被用于鉴定白色念珠菌8
。环己酰亚胺和氯霉素的结合能抑制很多致病菌2。但是,当在 25-30°C 下培养时,这些抗生素不会抑制荚膜组织胞浆菌、巴西副球孢子菌、申克孢子丝菌和皮炎芽生菌的菌丝相9。
在使用环己酰亚胺前,请检查相关的健康和安全文件。一些致病真菌可产生感染孢子,其很容易分散在实验室中。这类生物体只能在保护柜中进行检查。
部分国家或地区尚未销售赛默飞世尔科技的全部产品。详情请具体咨询。
Remel™ 和 Oxoid™ 产品现已归属 Thermo Scientific 品牌旗下,将强大的手动、半自动化以及全自动化检测产品与全面的培养基和诊断产品系列相结合,带来完整的端到端解决方案,能够快速交付您所需的产品以及您的实验室所倚重的高质量结果。
Georg 等人2在无菌条件下将 0.5g 环己酰亚胺、20,000 单位的青霉素和 40,000 单位的链霉素加入到每升经高温高压灭菌并冷却的培养基中。新型隐球菌、烟曲霉和波伊德氏霉杆真菌对环己酰亚胺敏感;牛放线菌和星形诺卡菌对青霉素和链霉素敏感。或者,可在高压灭菌前添加 0.4g 氯霉素和 0.05g 环己酰亚胺到每升再水化培养基中 (Ajello3)。同样的微生物对这一新的组合敏感(见皮肤真菌选择添加剂 SR0075E)。
Williams Smith & Jones4 采用 Oxoid 沙保氏葡萄糖琼脂,每升培养基含 20,000 单位青霉素和 0.04g 新霉素,用于猪消化道内的酵母菌计数。Hantschke5 使用粘菌素、新生霉素和环己酰亚胺分离白色念珠菌。Dolan6 使用庆大霉素、氯霉素和环己酰亚胺用于致病真菌的选择性分离。
Oxoid 沙氏葡萄糖琼脂也可以用作 Pagano-Levin 培养基的基质7,用于分离白色念珠菌。将 0.1g 氯化三苯基四氮唑(作为过滤灭菌溶液)添加到每升经高温高压灭菌然后冷却到 55°C 的熔融培养基中。通常通过加入抗生素将该培养基制成能抑制大多数非致病真菌和细菌的培养基,如上所述。在 25°C 下培养 3 天后,白色念珠菌菌落为未着色或浅粉色,而其他念珠菌属和其他真菌形成较深的粉色或红色菌落。该试验足以用于筛查目的,但其他的诊断标准也应被用于鉴定白色念珠菌8
。环己酰亚胺和氯霉素的结合能抑制很多致病菌2。但是,当在 25-30°C 下培养时,这些抗生素不会抑制荚膜组织胞浆菌、巴西副球孢子菌、申克孢子丝菌和皮炎芽生菌的菌丝相9。
在使用环己酰亚胺前,请检查相关的健康和安全文件。一些致病真菌可产生感染孢子,其很容易分散在实验室中。这类生物体只能在保护柜中进行检查。
部分国家或地区尚未销售赛默飞世尔科技的全部产品。详情请具体咨询。
Remel™ 和 Oxoid™ 产品现已归属 Thermo Scientific 品牌旗下,将强大的手动、半自动化以及全自动化检测产品与全面的培养基和诊断产品系列相结合,带来完整的端到端解决方案,能够快速交付您所需的产品以及您的实验室所倚重的高质量结果。
一般参考文献:
- Carlier Gwendoline I. M. (1948) Brit. J. Derm.Syph.60.61-63.
- Georg Lucille K., Ajello L. and Papageorge Calomira (1954) J. Lab.Clin.Med.44.422-428.
- Ajello Libero (1957) J. Chron.Dis.5.545-551.
- Williams Smith H. and Jones J. E. T. (1963) J. Path.Bact.86.387-412.
- Hantschke D. (1968) Mykosen.11.113-115.
- Dolan C. T. (1971) Appl.Microbiol.21.195-197.
- Pagano J., Levin J. G. and Trejo W. (1957-58) Antibiotics Annual 1957-58, 137-143.
- Kutscher A. H., Seguin L., Zegarelli E. V., Rankow R. M., Mercadante J. and Piro J. D. (1959a) J. Invest.Derm.33.41-47.
- McDonough E. S., Georg L. K., Ajello L. and Brinkman S. (1960) Mycopath.Mycol.Appl.13.113-116
规格
描述沙氏葡萄糖琼脂
数量2.5 kg
有效期每 5 年
形式粉末
产品类型Media Broth
Unit SizeEach
内容与储存
10°C 至 30°C