Search
SDS-PAGE蛋白凝胶电泳原理和实验步骤
蛋白凝胶电泳(SDS-PAGE)是一种在进行下游检测或分析前分离蛋白混合物的简单方法。我们提供高效的蛋白凝胶电泳方案,涵盖蛋白分析实验所需的蛋白预制胶、电泳槽、手灌胶系统、染料、蛋白Marker、电泳缓冲液、电泳仪电源和转印系统等产品。
什么是SDS-PAGE蛋白凝胶电泳?

蛋白凝胶电泳是一种在进行下游检测或分析前分离蛋白混合物的常规方法,在提取、鉴定和表征蛋白的众多工作流程中,蛋白凝胶电泳是非常关键的一个步骤。
电泳是指溶液中的带电颗粒在电场作用下发生移动的现象。电泳是一种可对蛋白和核酸进行简单、快速、灵敏的分离与分析的手段。任何带电离子或颗粒在电场作用下都会发生移动。多数生物分子在等电点以外的任何 pH 值下都带有净电荷,并且移动速度与电荷密度成正比。
凝胶基质
常用于电泳的基质有两种:聚丙烯酰胺凝胶和琼脂糖凝胶。这两种基质属于多孔介质,作用类似于分子筛。分子的分离度取决于基质的凝胶孔径大小。琼脂糖具有大孔径,是分离核酸和蛋白复合物等大分子的理想基质。聚丙烯酰胺的孔径较小,更适合分离大多数蛋白、肽段和较小的核酸。
聚丙烯酰胺凝胶电泳 (PAGE)
聚丙烯酰胺凝胶由丙烯酰胺单体聚合而成。这些单体在添加了能与链末端的自由官能团发生反应的双官能团化合物(如N,N’-亚甲基双丙烯酰胺,bis)后,可交联成长链。凝胶的孔径大小取决于丙烯酰胺和双丙烯酰胺的浓度。丙烯酰胺的浓度越高,凝胶孔径越小,这有助于提高低分子量分子的分辨率,反之亦然。
聚丙烯酰胺凝胶电泳可通过调整如下条件,根据不同应用需求来分离蛋白:
- 丙烯酰胺基质
- 缓冲液系统
- 电泳条件
丙烯酰胺基质
线性凝胶与梯度凝胶
具有单一丙烯酰胺百分比浓度的凝胶称为线性凝胶,丙烯酰胺浓度是某一范围的凝胶称为梯度凝胶。梯度凝胶相较于线性凝胶的优势为可在更宽的分子量范围内均匀地分离蛋白。
连续凝胶与非连续凝胶
研究人员有时会将凝胶分为连续凝胶和非连续凝胶。连续凝胶是在整个凝胶盒中采用单一丙烯酰胺溶液制作而成的凝胶。非连续凝胶则采用两种丙烯酰胺溶液制备:少量的低百分比浓缩胶(其中预留蛋白上样孔),以及大量的用于分离蛋白的分离胶。在传统的 Tris-甘氨酸蛋白凝胶系统中,浓缩胶位于高电泳迁移率的前导氯离子(存在于凝胶缓冲液中)与低电泳迁移率的甘氨酸尾随离子(存在于电泳缓冲液中)之间,蛋白在该浓缩胶中进行堆积。使用浓缩胶主要是为了提高凝胶中蛋白条带的分辨率。这些堆积的蛋白条带在进入分离胶后开始进行筛分。
小型蛋白凝胶与中型蛋白凝胶
我们提供两种规格的即用型预制胶:小型胶和中型胶。两种凝胶的电泳距离相同,但中型胶的尺寸更宽,因此上样孔数量更多或上样孔容量更大。中型胶中额外增加的上样孔数量或孔径,可以容纳更多样本数量或更高的样品体积。
缓冲液系统
电泳需要在连续或不连续的缓冲液系统中进行。连续缓冲系统使用同一种凝胶缓冲液和电泳缓冲液。不连续缓冲液系统使用不同的凝胶缓冲液和电泳缓冲液[1]。不连续缓冲液系统还可以使用两层孔径不同、缓冲液组分不同的凝胶层(浓缩胶和分离胶)。使用不连续缓冲液系统进行电泳可使样品在浓缩胶中堆积,从而获得更高的分辨率。
电泳条件
蛋白的分离方式取决于使用的电泳条件,下面介绍一些常见条件。
变性条件 (SDS-PAGE)
变性电泳是在使用阴离子去垢剂如十二烷基硫酸钠 (SDS)进行变性的条件下进行的电泳。SDS 通过包裹疏水部分使蛋白变性并展开。SDS 以 1 g 蛋白对应 1.4 g SDS 的比率结合。得到的 SDS-蛋白复合物带负电,按照分子大小在凝胶中分离。
非变性条件(天然 PAGE)
电泳是在非变性(天然)条件下,使用可以维持天然蛋白构象、亚基相互作用和生物学活性的缓冲液系统进行的电泳。在天然电泳过程中,蛋白的分离基于荷质比。
还原条件
使用还原剂,例如二硫苏糖醇 (DTT)、β-巯基乙醇 (β-ME)或盐酸三-(2-羧乙基)膦 (TCEP) 在还原条件下进行电泳。还原剂切割半胱氨酸残基之间的二硫键,将变性的蛋白完全展开,分解成亚基。
1D 和 2D PAGE 对比
蛋白凝胶电泳最常见的形式是采用一维 (1D) 电泳对多个样品进行比较分析。具体流程为:将样品加入上样孔中,施加电流分离蛋白,然后通过染色或免疫印迹将蛋白条带的迁移 情况可视化。
使用二维电泳 (2D-PAGE) 可以对单个样品的多个成分进行最彻底的解析。第一向等电聚焦 (IEF) 电泳根据蛋白的天然等电点 (pI) 分离蛋白。第二向电泳采用常规的 SDS-PAGE 根据分子量分离蛋白。2D-PAGE 可以为蛋白分析提供最高的分辨率,是蛋白组学研究中的一项重要技术。在这类研究中,有时需要在单块凝胶上解析成千上万种蛋白。
蛋白凝胶系统介绍
PAGE 利用不连续的缓冲液系统,在开始电泳时将样品浓缩或“堆积”到浓缩胶中非常窄的区域内。在不连续缓冲液系统中,凝胶中的主要阴离子与电泳缓冲液中的主要阴离子不同(或不连续)。Invitrogen™ Bolt™ Bis-Tris Plus 预制胶,Invitrogen™ NuPAGE™ Bis-Tris 和 Tris-乙酸预制胶,以及基于 Laemmli 系统的 Invitrogen™ Novex™ Tris-甘氨酸预制胶都是不连续缓冲液系统,具有类似的工作方式。但是,由于不同系统中的离子组成,Bis-Tris 和 Tris-乙酸系统需要在较低的 pH 值下工作。
Tris-甘氨酸系统
Tris-甘氨酸系统(图 1)主要包含如下三种离子:

图 1.Tris-甘氨酸预制胶系统。凝胶缓冲液中的离子为 Tris 和氯离子 (pH 8.7);电泳缓冲液中的离子为 Tris、甘氨酸和 SDS (pH 8.3) ;凝胶的工作 pH 值为 9.5。
- 凝胶缓冲液提供的氯化物 (–) 离子,作为前导离子(快离子),因为相对于系统中的其它阴离子,它对阳极的吸引力最高。
- 电泳缓冲液提供的甘氨酸 (–) 离子,是系统中的主要阴离因为这些离子仅部分带负电,并且在带电环境中始终跟随带电量更高的氯离子,因此作为尾随离子(慢离子)。
- Tris 碱 (+) 离子是一种在凝胶和电泳缓冲液中均存在的缓冲配对离子。电泳期间,Tris-甘氨酸系统中的凝胶和缓冲离子在凝胶的分离区域形成 pH 9.5 的工作环境。
Bis-Tris 系统
Bis-Tris 系统(图 2)主要包含如下三种离子:

图 2. Bis-Tris 预制胶系统。
- 由凝胶缓冲液提供的氯离子 (–),作为快速移动的前导离子。
- MES 或 MOPS (–) 离子(取决于电泳缓冲液的选择),作为尾随离子。
- MES:2-(N-吗啉代)乙烷磺酸
- MOPS:3-(N-吗啉代)丙烷磺酸
- 电泳缓冲液中提供Tris (+) 离子,凝胶中存在的 Bis-Tris (+)离子则为缓冲配对离子。
组合使用 pH 值较低的凝胶缓冲液 (pH 6.4) 和电泳缓冲液(pH 7.3–7.7),可在电泳过程中显著降低工作 pH (pH 7.0),从而实现更好的样品完整性和凝胶稳定性。
Tris-乙酸系统
Tris-乙酸系统(图 3)主要包含如下三种离子:
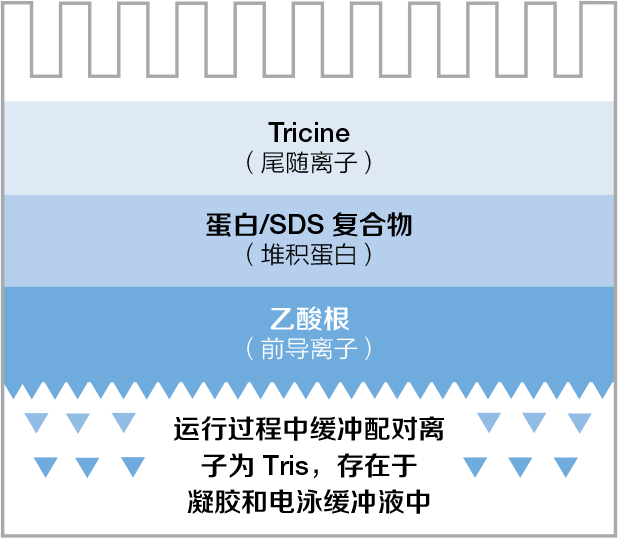
图 3. Tris-乙酸凝胶系统。
- 乙酸根 (–) 离子,来自凝胶缓冲液的前导离子
- Tricine (–) 离子,来自电泳缓冲液的尾随离子
- Tris (+) 离子,作为缓冲配对离子(凝胶和缓冲液中均存在)
该系统的工作 pH 值也比 Tris-甘氨酸系统低得多,从而减少了凝胶引发的蛋白修饰。
Tricine 系统
Tricine 系统是传统 Tris-甘氨酸凝胶系统的改进版本,使用了不连续缓冲液系统,专用于解析 2-20 kDa 范围的低分子量蛋白。通过重新配制 Laemmli 电泳缓冲液,并使用Tricine 代替甘氨酸,使 SDS -多肽在紧随前导离子前沿的位置形成,而不是与 SDS 前沿共同电泳,因此可以将它们分离为离散的条带。
实现理想蛋白分离的必备产品
蛋白预制胶
优化的蛋白凝胶体系,适用于宽范围的蛋白靶点分析。每种体系均有齐全的浓度和孔数选择,您也可选择手灌胶系统来手工制备蛋白凝胶。
电泳缓冲液
SDS-PAGE蛋白凝胶电泳缓冲液、非变性电泳缓冲液,以及用于制备手灌胶、凝胶上样、凝胶电泳和转印的试剂。
蛋白Marker
预染、非预染和 western blot 显影蛋白分子量标准。适用于SDS-PAGE、蛋白免疫印迹(western blot)和等电聚焦电泳(IEF)等。
蛋白凝胶染料
蛋白染料种类齐全,满足从快速染色到高灵敏度染色等应用所需。
赛默飞高品质蛋白电泳产品方案涵盖蛋白凝胶、蛋白染料、蛋白分子量标准、电泳缓冲液和转印设备等,可为您的不同实验需求提供针对性方案。
仅供科研使用,不可用于诊断目的。



