Search
PRR模式识别受体概述
什么是模式识别受体(PRR)?
先天免疫系统是宿主抵御病原微生物的第一道防线,并依赖于种系编码受体,也称为模式识别受体(PRR)[1,2,3]。这些受体识别在微生物上表达的分子特征,称为病原相关分子模式(PAMPs),以及在受损宿主细胞上表达的分子基序,称为损伤相关分子模式(DAMPs)[1,2,3]。PRR与PAMP和DAMP的相互作用可导致促炎细胞因子和其他免疫调节分子的表达 (图 1)[1,2,3]。PRR主要由抗原呈递细胞(APC)表达,包括树突状细胞和巨噬细胞,但它们也被发现在其他免疫细胞和非免疫细胞上表达[2,4]。
在哺乳动物的几种不同类型PRR中,Toll样受体(TLR)得到了相当广泛的研究 [2,4,5]。其他模式识别受体包括RIG-I样受体(RLR)、Nod样受体(NLR)、AIM2样受体(ALR)和C型凝集素受体(CLR),以及cGas和其他细胞内DNA传感器(图 1) [6,7,8]。这一概述主要为PRR的TLR和RLR类别。
图 1.先天免疫细胞(如树突状细胞和巨噬细胞)识别出各种病原体[2, 3, 4]。这些免疫细胞表达模式识别受体(PRR),它们能够识别病原诱导的感染是通过某些蛋白质和其他分子基序(称为病原相关分子模式(PAMP)和损害相关分子模式(DAMP)),而PAMP和DAMP分别是在病原体和受损宿主细胞上发现的[2, 3]。模式识别受体包括Toll样受体(TLR)、核苷酸结合的寡聚结构域样受体(Nod样受体,简称NLR)和C型凝集素受体(CLR)[6, 8]。
Toll样受体(TLR)信号通路
Toll样受体在先天免疫系统中发挥重要作用,主要是识别病原相关分子模式 [1,2,4,5]。Toll样受体由树突状细胞(DC)、巨噬细胞和非免疫细胞(如纤维原细胞)表达。Toll样受体可以根据其细胞位置进行分类[2,3,4]。人的TLR家族由10个成员组成(TLR1-TLR10),而小鼠TLR家族有12个成员(TLR1-TLR9, TLR11-TLR13)。细胞表面TLR包括TLR1、TLR2、TLR4、TLR5、TLR6和TLR10,并都有胞外的结构域 [2,3,4]。胞内TLR包括TLR3、TLR7、TLR8、TLR9、TLR11、TLR12和TLR13,它们位于内质网(ER)、内体和溶酶体中 [2,6,7]。细胞表面TLR识别细菌膜成分,如脂质、脂蛋白和蛋白质,而细胞内TLR主要识别核酸[8,9]。TLR识别的PAMP部分清单,见表 1。
TLR被认为是I型跨膜蛋白,由一个N端配体识别域、一个单次跨膜域和一个C端信号域组成[10]。TLR的胞外域包含一段基序的串联拷贝,也称为富含亮氨酸重复结构(LRR),负责识别PAMP[10]。TLR的细胞内信号域与IL-1受体同源,被称为Toll/interukin-1受体(TIR)域[10]。这个信号域是发起下游信号通路所必需的10。TLR激活相关的两个主要信号通路包括MyD88依赖通路和TRIF依赖通路(图 2) [10]。
图 2.病原通过TLR在APC上激发的信号通路。像TLR1这样的细胞表面TLR具有胞外域,而像TLR3这样的细胞内TLR是位于胞内的 [2, 6, 10]。同源或异源二聚体的形成能够诱导下游信号通路,主要是MyD88依赖通路或者TRIF依赖通路[10]。TLR的下游通路引起促炎细胞因子的表达,包括白细胞介素-6(IL-6)、IL-8、IL-12和肿瘤坏死因子alpha(TNFα)[10]。
表 1.Toll样受体(TLR)识别的病原相关分子模式(PAMP) [8]。
| TLR型(结构) | 衔接蛋白(结构) | PAMP/激活蛋白 | 物种 |
|---|---|---|---|
| TLR1-TLR2 (LRR-TIR) | MyD88(TIR-DD), TIRAP(TIR) | Triacyl lipopeptides | Bacteria |
| TLR2–TLR6(LRR–TIR) | MyD88 TIRAP | Diacyl lipopeptides LTA Zymosan | Mycoplasma Bacteria Fungus |
| TLR2(LRR–TIR) | MyD88, TIRAP | PGN Lipoarabinomannan Porins tGPI-mucin HA protein | Bacteria Mycobacteria Bacteria (Neisseria) Parasites (Trypanosoma) Virus (measles virus) |
| TLR3(LRR–TIR) | TRIF(TIR) | dsRNA | Virus |
| TLR4(LRR–TIR) | MyD88, TIRAP, TRIF, TRAM (TIR) | LPS Envelope proteins | Bacteria Virus (RSV, MMTV) |
| TLR5 (LRR–TIR) | MyD88 | Flagellin | Bacteria |
| TLR7 (LRR–TIR) | MyD88 | ssRNA | RNA virus |
| hTLR8 (LRR–TIR) | MyD88 | ssRNA | RNA virus |
| TLR9 (LRR–TIR) | MyD88 | CpG DNA DNA Malaria hemozoin | Bacteria DNA virus Parasites |
| mTLR11 (LRR–TIR) | MyD88 | Not determined Profilin-like molecule | Bacteria (uropathogenic bacteria) Parasites (Toxoplasma gondii) |
缩写: dsRNA,双链核糖核酸;HA,血凝素;LPS,脂多糖;LRR,富亮氨酸重复;LTA,脂磷壁酸;MMTV,小鼠乳腺肿瘤病毒;MyD88,髓系分化原发反应88;PGN,肽聚糖;RSV,呼吸道合胞病毒;ssRNA,单链核糖核酸;tGPI-粘蛋白(糖基磷脂酰肌醇锚定的粘蛋白样糖蛋白);TIR,Toll/白细胞介素-1受体;TIRAP,含衔接蛋白的TIR域;TLR,Toll样受体;TRIF,含衔接子诱导干扰素-β的TIR域;TRAM,TRIF相关衔接分子。 | |||
RIG-I样受体(RLR)信号通路
虽然胞内检测TLR RNA有助于抗病毒免疫,但是RLR对于多数RNA病毒的免疫识别和应答至关重要 [11,12]。RLR主要识别单链RNA和双链RNA(ssRNA和dsRNA)。RLR家族的受体成员可以在所有细胞类型的细胞质中找到,并且由RIG-I(retinoic acid-inducible gene I)、MDA5(melanoma differentiation-assoicated gene 5)和LGP2(laboratory of genetics and physiology 2)组成 [13,14]。当出现病毒感染或存在细菌RNA时,RIG-I和MDA5能够诱导产生I型干扰素(IFN)和趋化因子。
RLR通常由两个N端半胱天冬酶募集域(CARD)、一个中心DEAD盒解旋酶/ATPase域和一个C端调节域组成 [12,13,14]。LGP2不含CARD域,因此其对下游抗病毒信号的影响可能是因为LGP2与dsRNA病毒配体的作用或与其他RLR(RIG-I和MDA5)的相互作用产生的。RLR位于细胞质中,能够识别dsRNA病毒的基因组RNA,也能识别ssRNA病毒复制中间体产生的dsRNA [15,16]。在IFN I型刺激或病毒感染的应答中,RLR的表达大幅增强 [13,14,15]。病毒RNA刺激RIG-I或MDA5表达相关的CARD域,这些域与K63多泛素链聚集成CARD四聚体,然后结合并激活衔接分子MAVS。MAVS募集TBK-1,TBK-1磷酸化IRF3,最终诱导I型干扰素基因的转录 [13,14,15]。
在Toll样受体(TLR)敲除小鼠中研究PRR通路
PRR通路对于建立抗微生物感染的有效防御是不可或缺的。一些研究调查了微生物病原体与其影响先天免疫系统之间的关系 [17,18]。
Qureshi 等人研究了小鼠对细菌脂多糖(LPS)的应答 [17,18]。他们的数据显示,对LPS应答的调节位于小鼠4号染色体上编码TLR4的 Lps 位点。这项研究确定TLR4是宿主对致病性LPS应答的关键调节分子 [17,18]。
Oosting 等人研究了TLR1/TLR2异二聚体之间的关系和它们对包柔氏螺旋体属的应答[19]。TLR2的一个重要特征是它可以与TLR1和TRL6形成异二聚体 [19]。尽管TLR2被认为是包柔氏螺旋体属的主要受体,但有证据表明TLR1和TLR6发挥了作用[19]。TLR1和TLR6基因敲除小鼠被分别暴露于包柔氏螺旋体中。TLR1基因敲除小鼠表现出干扰素γ的表达增加,这与TLR6基因敲除小鼠相反,后者不能产生明显的干扰素γ应答。在两个敲除品系之间的促炎细胞因子中没有显著变化[19]。
Toll样受体(TLR)免疫学研究
TLR是病原体检测中至关重要的传感器,因此识别和表征免疫细胞表面的TLR表达对于研究病毒清除的细胞机制具有重要意义。流式细胞仪通常是分析免疫细胞TLR谱的首选方法。
一般来说,整个细胞群用活性染料染色,然后用TLR特异性荧光抗体进行免疫标记。为了对单细胞悬液中的所有活细胞进行染色,用磷酸盐缓冲盐水(PBS)冲洗一次,并以1×106个/mL重悬于染色缓冲液中,如Invitrogen Bioscience流式染色缓冲液。接下来,向细胞悬液中加入1 µL活性染料,如 Invitrogen可固定活性染料。然后将细胞在室温或冰上避光培养30分钟,用1 mL PBS冲洗一次,并重悬在100 µL染色液中。
TLR1、TLR2、TLR4、TLR5、TLR6和TLR10,这些TLR在细胞表面有胞外域,因此可直接用荧光抗体识别目标TLR(或光谱兼容的荧光抗体)对细胞染色(图 3,表2)。细胞在冰上培养30分钟,用染色缓冲液冲洗,然后重悬在300 µL染色液中。可以用流式细胞仪进来分析细胞,如Invitrogen Attune NxT 流式细胞仪。如果上样前需要固定细胞,可以使用固定缓冲液,如Invitrogen eBioscience 胞内固定缓冲液。在短暂培养后,将细胞冲洗并重悬于染色缓冲液中,再上样到流式细胞仪。
TLR3、TLR7、TLR8、TLR9、TLR11、TLR12和TLR13,这些细胞内TLR的抗体染色,细胞必须固定并破膜,使抗体与抗原接触。细胞已经免疫标记了细胞表面抗原,如上所述再进行固定,并使用破膜缓冲液进行破膜,如 Invitrogen eBioscience破膜缓冲液。完成固定和破膜后,细胞与识别相关TLR的荧光抗体试剂(或光谱相容的其他荧光抗体)一起培养 (表2)。细胞与抗体在冰上培养 30 分钟,用破膜缓冲液冲洗一次,用染色缓冲液冲洗一次,然后重悬于300 µL染色缓冲液中。重新悬浮后,可以通过流式细胞仪来分析细胞。
由于免疫细胞上高密度的Fc受体,背景荧光可能是个问题 [4]。我们建议使用未标记阻断抗体,如人类细胞的Invitrogen Fc 受体结合抑制剂多克隆抗体,或小鼠细胞的Invitrogen CD16/CD32 单克隆抗体 (clone 93)和Invitrogen正常大鼠血清。
在检测核内靶标中,例如NF-κB和其他转录因子的抗体标记(表2),我们建议使用Invitrogen eBioscience FoxP3/转录因子染色缓冲液来固定和破膜这些细胞(在上一步骤可能免疫标记了细胞表面抗原)。在固定和破膜后,细胞与一个或多个荧光抗体共同培养,这些荧光抗体能够识别这些转录因子。细胞在冰上培养30分钟,用FoxP3/转录因子染色缓冲液的破膜缓冲液冲洗一次、用染色缓冲液冲洗一次,然后重新悬浮于300 µL染色缓冲液中。重新悬浮后,可以通过流式细胞仪来分析细胞。
表 2.TLR标志物及其检测方法的部分列表[2, 4, 10]。
| TLR标志物 | 检测方法 |
|---|---|
| 胞外/胞膜标志物 | |
| TLR1 | WB, IHC, ICC, IF, Flow |
| TLR2 | WB, IHC, ICC, IF, Flow |
| TLR4 | WB, IHC, ICC, IF, Flow |
| TLR5 | WB, IHC, ICC, IF, Flow |
| TLR10 | WB, IHC, ICC, IF, Flow |
| 细胞内标志物 | |
| TLR6 | WB, IHC, ICC, IF, Flow |
| TLR7 | WB, IHC, ICC, IF, Flow |
| TLR8 | WB, IHC, ICC, IF, Flow |
| TLR9 | WB, IHC, ICC, IF, Flow |
| TLR11 | WB, IHC, ICC, IF, Flow |
| TLR12 | WB, IHC, ICC, IF, Flow |
| TLR13 | WB, IHC, ICC, IF, Flow |
| NF-κB | WB, IHC, ICC, IF, Flow, ChIP |
| 细胞因子 | |
| IFNγ | WB, IHC, ICC, IF, ELISA |
| TNFα | WB, IHC, ICC, IF, ELISA |
| IL-6 | WB, IHC, ICC, IF, ELISA |
| IL-8 | WB, IHC, ICC, IF, ELISA |
| IL-12 | WB, IHC, ICC, IF, ELISA |
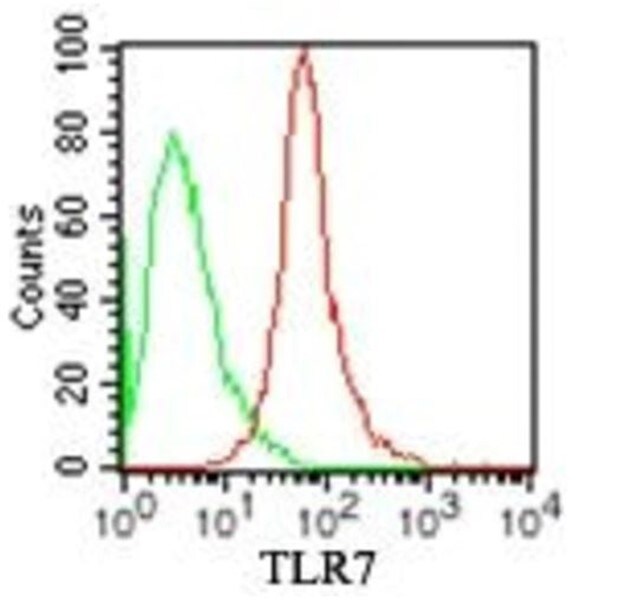
图 3.使用10 µL(0.5 µg)Invitrogen TLR7单克隆抗体,PE标记(Clone: 4G6,Cat. No. MA5-16249)(红色)和0.5 µg小鼠 IgG1同型对照(绿色)对1 x 106人类BDCM(具有 DC 形态的B细胞)中的TLR7进行流式胞内分析。
- Kawai T, Akira S (2010) The role of pattern-recognition receptors in innate immunity: Update on Toll-like receptors.Nat Immunol 11(5), 373–384.
- Kawasaki T, Kawai T (2014) Toll-like receptor signaling pathways.Front Immunol 5:461.
- Celhar T, Magalhães R, Fairhurst AM (2012) TLR7 and TLR9 in SLE: When sensing self goes wrong.Immunol Res 53(1-3):58–77.
- Andersen MN, Al-Karradi SNH, Kragstrup TW et al.(2016) Elimination of erroneous results in flow cytometry caused by antibody binding to Fc receptors on human monocytes and macrophages.Cytometry A 89(11):1001–1009.
- Abdi J, Mutis T, Garssen J et al.(2013) Characterization of the Toll-like receptor expression profile in human multiple myeloma cells.PLoS One 8(4):e60671.
- Amarante-Mendes GP, Adjemian S, Branco LM et al.(2018) Pattern recognition receptors and the host cell death molecular machinery.Front Immunol 9:2379.
- Janeway CA, Medzhitov R (2002) Innate immune recognition.Annu Rev Immunol 20(1):197–216.
- Kawai T, Akira S (2009) The roles of TLRs, RLRs and NLRs in pathogen recognition.Int Immunol 21(4):317–337.
- Pattern recognition receptor (PRRs) ligands.British Society for Immunology.Retrieved March 1, 2021
- Botos I, Segal DM, Davies DR (2011) The structural biology of Toll-like receptors.Structure 19(4):447–459.
- Saito T, Hirai R, Loo YM et al.(2007) Regulation of innate antiviral defenses through a shared repressor domain in RIG-I and LGP2.Proc Natl Acad Sci U S A 104(2):582–587.
- Schlee M (2013) Master sensors of pathogenic RNA—RIG-I like receptors.Immunobiology 218(11):1322–1335.
- Loo YM, Gale M Jr (2011) Immune signaling by RIG-I-like receptors.Immunity 34(5):680–692
- Ivashkiv LB, Donlin LT (2014) Regulation of type I interferon responses.Nat Rev Immunol 14(1):36–49.
- Kato H, Sato S, Yoneyama M et al.(2005) Cell type–specific involvement of RIG-I in antiviral response.Immunity 23(1):19-28.
- Kato, Hiroki (2006) Differential role of MDA5 and RIG-I in the recognition of RNA viruses.Nature.441(7089), 101-105
- Qureshi ST, Medzhitov R (2003) Toll-like receptors and their role in experimental models of microbial infection.Genes Immun 4(2):87–94.
- Qureshi,ST, Gros P, Malo D (1999) The Lps locus: Genetic regulation of host responses to bacterial lipopolysaccharide.Inflamm Res 48(12):613–620.
- Oosting M, Ter Hofstede H, Sturm P et al.(2011) TLR1/TLR2 heterodimers play an important role in the recognition of Borrelia Spirochetes.PLoS One 6(10):e25998.
仅供科研使用,不可用于诊断目的。





