Search
pull-down实验
pull-down实验简介
pull-down实验是一种体外方法,用于确定两个或多个蛋白质之间的物理相互作用。pull-down实验既可用于确认其他研究技术(如共免疫沉淀)预测的蛋白质-蛋白质相互作用的存在,也可作为初步筛选实验,用于发现以前未知的蛋白质-蛋白质相互作用。
pull-down实验是一种亲和纯化形式,与免疫沉淀类似,但使用“诱饵”蛋白而不是抗体。亲和层析(即亲和纯化)方法极大地提高了蛋白质纯化的速度和效率,同时为进行pull-down或共纯化潜在结合伙伴提供了技术平台。在pull-down实验中,诱饵蛋白被标记并捕获在针对该标签的固定亲和配体上,从而生成用于纯化与诱饵蛋白相互作用的其他蛋白的“二级亲和支持”。固定诱饵的二级亲和支持随后与含有假定“猎物”蛋白的蛋白来源(如细胞裂解液)一起孵育。在此步骤中猎物蛋白的来源取决于研究人员是确认先前怀疑的蛋白质-蛋白质相互作用,还是识别未知的相互作用。蛋白质的洗脱方法取决于亲和配体,范围包括使用竞争性分析物、低pH或还原缓冲液。
除了研究两个或多个蛋白质的相互作用外,pull-down实验还是检测特定蛋白质激活状态的强大工具。例如,对酪氨酸磷酸化有反应而被激活的蛋白质,可以通过使用固定的SH2结构域(该结构域靶向特定蛋白上的磷酸化酪氨酸)进行pull-down。此外,GTP酶作为分子开关,通过在GTP结合(活性)和GDP结合(非活性)状态之间循环来调节细胞信号转导,可以通过使用固定的下游蛋白的GTP酶结合结构域(这些蛋白被招募到GTP结合的活性GTP酶上)进行pull-down。在这两种类型的pull-down实验中,由于相互作用的特异性取决于结合结构域的序列,这些方法在检测不同蛋白质的激活方面具有高度特异性。
蛋白质制备手册
在这本 32 页的手册中,您可以了解更多有关如何使用各种 Thermo Scientific 蛋白生物学工具对蛋白质样品进行脱盐、缓冲液交换、浓缩和/或去除杂质、免疫沉淀以及其他蛋白质纯化和清理方法的信息。
- 免疫沉淀 (IP)、共同 IP 和染色质-IP
- 重组蛋白纯化标签
- 使用 Slide-A-Lyzer 透析盒和装置安全地透析蛋白质样品
- 使用 Zeba 自旋脱盐柱和板快速脱盐样品,提高蛋白质回收率
- 使用针对去除洗涤剂或内毒素而优化的树脂有效提取特定污染物
- 使用 Pierce 蛋白浓缩器快速浓缩稀释蛋白质样品
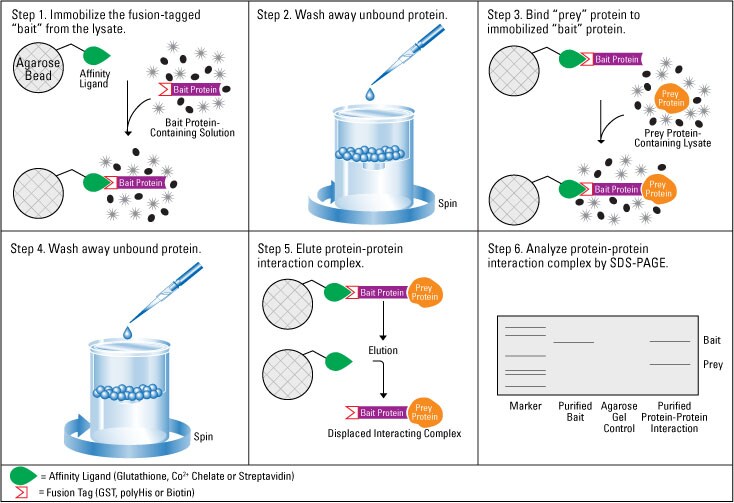
pull-down实验的一般示意图 pull-down实验是一种小规模的亲和纯化技术,类似于免疫沉淀,但抗体被其他亲和系统所替代。在这种情况下,亲和系统由谷胱甘肽S-转移酶(GST)、多组氨酸(polyHis)或链霉亲和素标签蛋白或结合域组成,分别通过谷胱甘肽、金属螯合物(钴或镍)或生物素包被的琼脂糖珠捕获。固定化的融合标签蛋白作为“诱饵”,用于捕获假定的结合伙伴(即“猎物”)。在典型的pull-down实验中,固定化的诱饵蛋白与细胞裂解液孵育,经过规定的洗涤步骤后,使用竞争性分析物或低pH值或还原缓冲液选择性洗脱复合物,以进行凝胶内或蛋白印迹分析。
pull-down实验作为验证⼯具
对先前推测的相互作⽤进⾏确认时,通常使⽤在⼈⼯蛋⽩表达系统中表达的猎物蛋⽩作为来源。这使研究⼈员能够获得数量更多的蛋⽩,相较于内源性表达条件,并避免由于诱饵与内源系统中其他未研究的相互作⽤蛋⽩发⽣相互作⽤⽽导致的混淆结果。适用于验证性研究的猎物蛋白来源包括:蛋白表达体系裂解物(如 E. coli 或杆状病毒感染的昆虫细胞)、体外转录/翻译反应产物,以及预先纯化的蛋白。
pull-down实验作为探索⼯具
发现未知相互作⽤与验证性研究不同,作为发现工具的 pull-down 实验旨在鉴定在内源环境中与特定诱饵蛋白(bait protein)发生相互作用的未知蛋白。内源环境可能包含⼤量潜在的蛋⽩来源,但通常被认为是诱饵蛋⽩的天然环境的复杂蛋⽩混合物。任何诱饵蛋⽩正常表达的细胞裂解液,或诱饵蛋⽩可能发挥功能的复杂⽣物液体(如 ⾎液、肠道分泌物等),都是⽤于发现性研究的合适猎物蛋⽩来源。
pull-down实验的关键组成部分
诱饵蛋白标准
用于 pull-down 实验 的诱饵蛋白(bait protein)可以通过两种主要方式获得:一是将亲和标签连接到通过传统纯化方法获得的蛋白;二是表达重组的融合标签蛋白。研究⼈员如果能够获得市售的纯化蛋⽩或前期实验中冻存的纯化蛋⽩样品,可以在⽆需克隆⽬标蛋⽩编码基因的情况下设计pull down实验。纯化蛋⽩可以⽤常⽤于此类标记应⽤的蛋⽩反应性标签进⾏标记。另一方面,如果目标基因已完成克隆,可以采⽤分⼦⽣物学⽅法将该基因亚克隆到带有融合标签的合适载体中。重组克隆可以⾼效表达并容易纯化,从⽽获得⼤量⽤于pull down实验的诱饵蛋⽩。在下述代表性⽰例中,⾕胱⽢肽-S-转移酶(GST)被⽤于进⾏pull down实验。
常见融合标签及其亲和配体
| 融合标签 | 亲和配体 |
|---|---|
| 谷胱甘肽-S-转移酶 (GST) | 谷胱甘肽 |
| 多组氨酸 (polyHis or 6xHis) | 镍或钴螯合物 |
| 生物素 | 链霉亲和素 |

利用固定化谷胱甘肽纯化N端GST融合蛋白 克隆到pT7CFE1-NHis-GST-CHA中的基因用于表达GST融合蛋白,表达时间为6小时。蛋白与Thermo Scientific Pierce谷胱甘肽琼脂糖结合后,用50 mM谷胱甘肽洗脱GST融合蛋白。纯化蛋白中出现的额外条带(用箭头标注)此前已通过质谱鉴定为细胞蛋白eEF1G和GSTM3,这两种蛋白已知能与谷胱甘肽柱结合,并与GST标签蛋白共同洗脱。每种纯化蛋白约500 ng通过SDS-PAGE分离,并用Thermo Scientific Pierce Power Stainer(货号:22833)染色。缩写说明:His:6X组氨酸重复;GST:谷胱甘肽S转移酶;HRV3c位点:人鼻病毒3C蛋白酶位点;GOI:目标基因;HA:血凝素序列;BSA:牛血清白蛋白;GFP:绿色荧光蛋白;CAV1:洞蛋白1;BAD:Bcl-2相关死亡促进因子;Green Renilla:绿色Renilla荧光素酶;CCND1:周期素D1;Guassia:Guassia荧光素酶;AKT3:蛋白激酶;AGO2:Argonaute RISC催化组分2;RB1:视网膜母细胞瘤蛋白1。
结合参数:稳定与瞬时相互作用
蛋白质-蛋白质相互作用的发现和确认依赖于所研究相互作用的性质,使用pull-down技术时尤为如此。相互作用可以是稳定的或瞬时的,这一特性决定了诱饵蛋白与猎物蛋白结合条件的优化方式。瞬时相互作用通常与运输或酶促机制相关。核糖体就是两者的例子,因为其结构包含许多稳定的蛋白质-蛋白质相互作用,但将mRNA翻译为新生蛋白的酶促机制则需要瞬时相互作用。
稳定的蛋白质-蛋白质相互作用最容易通过pull-down等物理方法分离,因为蛋白质复合物不会随着时间解离。强而稳定的蛋白质复合物可以用高离子强度缓冲液充分洗涤,以消除由于非特异性相互作用导致的假阳性结果。如果复合物的解离常数较高、相互作用较弱,则可以通过优化与pH值、盐种类和盐浓度相关的实验条件,提高相互作用强度和蛋白质复合物的回收率。通过精心设计合适的对照实验,可以最大限度地减少非特异性相互作用的问题。以下为利用专用试剂盒进行pull-down活性Cdc42的实验设计示例。

活性Cdc42的检测. The 活性Cdc42pull-down和检测试剂盒 检测经GTPγS(激活剂)或GDP(失活剂)处理的NIH 3T3细胞裂解液中的活性蛋白。通过pull-down实验富集活性Cdc42。每份洗脱液的一半(25 µL)及40 µg总裂解液用试剂盒提供的抗Cdc42抗体进行蛋白免疫印迹分析。仅检测到活性Cdc42,如GDP处理样品信号强度较低所示。
瞬时相互作⽤是指蛋⽩质之间的时间性相互作⽤,是最难分离的蛋⽩质-蛋⽩质相互作⽤类型。这类相互作⽤⽤pull-down等物理⽅法更难识别,因为复合物可能在实验过程中解离。由于瞬时相互作⽤发⽣在运输过程中或作为酶促过程的⼀部分,通常需要辅因⼦和通过核苷三磷酸⽔解提供的能量。在实验优化过程中加⼊辅因⼦和不可⽔解的核苷三磷酸(NTP)类似物,可以“捕获”依赖于辅因⼦或NTP的功能复合物不同阶段的相互作⽤蛋⽩。
弱或瞬时的蛋⽩质–蛋⽩质相互作⽤可以通过在pull-down实验前将相互作⽤的蛋⽩质共价交联来增强。尽管与不使用交联剂的常规 pull-down 实验相比,这一策略在技术上更为复杂,但通过交联“冻结”蛋白之间的相互作用,往往能够显著提高实验成功率。在某些情况下,是否采用交联步骤甚至可能成为 pull-down 实验成败的关键因素。
诱饵–猎物复合物的洗脱
要鉴定诱饵–猎物相互作⽤,需要将复合物从亲和载体上移除,并通过标准蛋⽩检测⽅法进⾏分析。常用的洗脱方式主要有两类:SDS-PAGE 上样缓冲液洗脱 和 针对诱饵蛋白标签的竞争性分析物洗脱。SDS-PAGE上样缓冲液是⼀种强烈处理⽅式,会使样品中的所有蛋⽩质变性,并且仅限于SDS-PAGE分析。此外,这种强洗脱方式不仅会释放特异性结合的诱饵–猎物复合物,还可能将非特异性吸附在亲和基质上的多余蛋白一并洗脱下来,从而增加背景信号,干扰后续的数据分析和结果判读。竞争性分析物洗脱对诱饵–猎物相互作⽤更具特异性,因为它不会剥离⾮特异性结合在亲和载体上的蛋⽩质。这种⽅法是⾮变性的,因此可以洗脱出具有⽣物学功能的蛋⽩复合物,这对于后续研究可能⾮常有⽤。
另⼀种洗脱⽅案是使⽤逐步增加盐浓度或降低pH值的梯度,这允许选择性地洗脱猎物蛋⽩,⽽诱饵蛋⽩仍然固定在载体上。⼀旦为⾼效洗脱优化了临界盐浓度或pH值,就不再需要梯度洗脱。这些洗脱⽅法同样是⾮变性的,并且有助于判断相互作⽤的相对强度。
凝胶检测诱饵–猎物复合物
通常通过SDS-PAGE检测洗脱液中是否存在猎物蛋白,随后进行总蛋白染色或蛋白质印迹(western blot)分析。总蛋白染色(如考马斯亮蓝染色、银染或锌染)可以显示洗脱液中的所有蛋白质,通过分子量识别猎物蛋白。蛋白质印迹分析更具特异性和灵敏度,因为它使用抗体来检测猎物蛋白。
pull-down实验的对照
pull-down实验(Pull-down assays)通常包括多个步骤,往往需要使用不止一种细胞裂解液,因此每个实验都必须进行适当的对照,以证明最终结果不是人为造成的假象。每次实验都应在裂解液通过载体之前和之后进行分析,以识别是否存在对载体的非特异性结合。每次洗涤也应进行分析,以观察是否有蛋白质被洗脱,同时还应设置无诱饵和无猎物的对照,以确认在诱饵裂解液中不存在诱饵-猎物相互作用,并且猎物蛋白不会与固定化载体结合。
pull-down方法学
自制的 pull-down 方法被广泛用于验证或发现蛋白–蛋白相互作用,在当代科学文献中十分常见。然而,自制 pull-down 实验通常需要将来自多个商业供应商的试剂组合使用,这些试剂作为一个完整体系并未经过整体功能验证,研究人员只能通过大量的实验优化来加以验证;同时,这种多试剂组合在排错过程中往往繁琐且耗时。商业化的pull-down实验试剂盒则包含了专⻔为pull-down实验开发的完整、经过验证的试剂套装。每个试剂盒中提供的缓冲液允许⽤⼾灵活确定分离相互作⽤蛋⽩的最佳条件。⽤于洗涤和结合的⼯作液在pH值和离⼦强度上均为⽣理条件,为优化每⼀对独特相互作⽤蛋⽩的特定缓冲条件提供了起点。许多商业试剂盒还配备了离⼼柱,便于⾼效处理⼩体积亲和载体,确保pull-down实验过程中亲和载体的完全保留,并能彻底洗涤蛋⽩复合物,从⽽最⼤限度减少⾮特异性蛋⽩pull-down,这些都是传统pull-down 实验⽅法中常⻅的变异和⾼背景来源。
了解更多
- 蛋白质相互作用分析
- 技术指南 #64: 免疫沉淀(IP)技术指南与实验方案
- 应用说明 : 计算琼脂糖亲和载体上每颗珠子的固定化蛋白数量
- 蛋白免疫沉淀(IP)、共免疫沉淀(Co-IP)及Pull-Down实验支持
Recommended reading
- Einarson MB, Orlinick JR (2002) Identification of Protein-Protein Interactions with Glutathione S-Transferase Fusion Proteins. In: Protein-Protein Interactions: A Molecular Cloning Manual. Cold Spring Harbor (NY): Cold Spring Harbor Laboratory Press. pp 37–57.
- Einarson MB (2001) Detection of Protein-Protein Interactions Using the GST Fusion Protein Pulldown Technique. In: Molecular Cloning: A Laboratory Manual, 3rd Edition. Cold Spring Harbor (NY): Cold Spring Harbor Laboratory Press. pp 18.55–18.59.
- Vikis HG, Guan K-L (2004) Glutathione-S-Transferase-Fusion Based Assays for Studying Protein-Protein Interactions. In: Fu H (editor), Protein-Protein Interactions, Methods and Applications, Methods in Molecular Biology, 261. Totowa (NJ): Humana Press. pp 175–186.
仅供科研使用,不可用于诊断目的。
