Search
质谱分析中的肽段富集与分馏技术
在蛋白质酶解后,肽段的富集(Enrichment)和/或分馏(Fractionation)通常是检测低丰度蛋白肽段或降低样本复杂性的必要步骤。提升目标蛋白鉴定率的常用策略包括:翻译后修饰(PTM)特异性富集, 例如:磷酸化肽段富集;或分馏技术, 例如:根据肽段疏水性差异分离的高pH反相色谱法。
创新的Thermo Scientific ™ActivX™探针与富集试剂盒能特异性地靶向多种酶类,包括激酶、GTP 酶和丝氨酸水解酶,通过在蛋白质水平对其活性位点进行共价标记,并在酶解后实现高效富集。
- 全面性:提供多种肽段富集/分馏策略的试剂与试剂盒。
- 优化设计:最大化蛋白得率,提升目标蛋白鉴定数量。
- 便捷操作:离心柱、吸头或磁珠形式简化样本处理流程。
- 灵活适配:适用于培养的哺乳动物细胞或组织样本。
- 严格验证:所有产品均经Thermo Scientific™质谱平台测试,确保数据可靠性。
为您的应用选择合适的肽段富集或分馏产品
磷酸化是一种重要的蛋白质修饰形式,参与细胞信号传导、生长、分化、分裂以及程序性细胞死亡等多种生物学过程。然而,磷酸肽通常具有较强的亲水性且丰度较低,导致其在色谱分离、电离及碎裂过程中的表现较差。因此,磷酸肽富集是实现成功质谱分析的关键步骤。
金属氧化物亲和色谱(MOAC)和固定化金属离子亲和色谱(IMAC)是目前最常用的两种磷酸肽富集方法。由于这两种方法对不同类型的磷酸肽序列具有选择性,我们提供多种柱式、吸头及试剂盒产品,以满足不同研究应用和实验目标的需求。
磷酸化肽富集试剂盒
 |  |  |  |  | |
|---|---|---|---|---|---|
| Fe-NTA磁珠法磷酸肽富集试剂盒 | Fe-NTA 磷酸肽富集试剂盒 | TiO2 磷酸肽富集与纯化试剂盒 | 石墨离心柱 | TiO2 磷酸肽富集吸头 | |
| 结合/标记机制 | 金属螯合物对磷酸基团的亲和作用 | 金属螯合物对磷酸基团的亲和作用 | 金属氧化物对磷酸基团的亲和作用 | 石墨对亲水性肽的亲和作用 | 金属氧化物对磷酸基团的亲和作用 |
| 富集策略 | Fe-NTA 磁珠 | IMAC琼脂糖树脂 | 球形多孔 TiO2 | 石墨离心柱 | 球形多孔 TiO2 |
| 上样量/反应* | 25–1,000 µg | 0.5–5 mg | 0.5–3 mg | 100 µg | 300–1,000 µg |
| 形式 | 磁珠 | 离心柱 | 吸头 | 离心柱 | 离心吸头 |
| 处理时间 | <45 分钟 | 45–60 分钟 | 45–60 分钟 | 10–20 分钟 | 35–45 分钟 |
| 立即订购 | 立即订购 | 立即订购 | 立即订购 | 立即订购 |
*每次反应的上样量基于典型哺乳动物培养细胞蛋白酶解样品计算
Thermo Scientific Pierce 激酶富集试剂盒采用 ActivX™ ATP 或 ADP 探针,对 ATP 酶(包括激酶、分子伴侣及代谢酶)活性位点进行共价标记。该类探针包含一种可与胺基反应的核苷酸类似物,以及一个 desthiobiotin(去硫生物素,生物素类似物)标签,从而实现对激酶活性位点中赖氨酸残基的选择性标记,并可进一步对已标记蛋白进行富集与回收。
这些特性使其能够用于不同样品中目标酶类别的鉴定与谱分析,或用于评估酶抑制剂的特异性和亲和力。
在质谱工作流程中,desthiobiotin 标记的蛋白首先进行还原、烷基化处理,并经酶解生成肽段。随后,仅对携带 desthiobiotin 标记的活性位点肽进行富集,并通过 LC-MS/MS 进行分析,从而实现对抑制剂全局靶点及潜在脱靶的鉴定。
激酶富集试剂盒
 | ||
|---|---|---|
| ATP 探针激酶富集试剂盒 | ADP 探针激酶富集试剂盒 | |
| 结合/标记机制 | 生物素化 ATP 类似物与活性位点赖氨酸结合 | 生物素化 ADP 类似物与活性位点赖氨酸结合 |
| 富集策略 | 固定化链霉亲和素琼脂糖树脂 | 固定化链霉亲和素琼脂糖树脂 |
| 上样量/反应* | 冻干形式(Lyophilized) | |
| 形式 | 离心柱 | 离心柱 |
| # 洗脱级分数 | 1 | 1 |
| 处理时间 | 6.5 小时 + 酶解 | 6.5 小时 + 酶解 |
| 立即订购 | 立即订购 |
磷酸化是一种重要的蛋白质修饰形式,参与细胞信号传导、生长、分化、分裂以及程序性细胞死亡等多种生物学过程。然而,磷酸肽通常具有较强的亲水性且丰度较低,导致其在色谱分离、电离及碎裂过程中的表现较差。因此,磷酸肽富集是实现成功质谱分析的关键步骤。
金属氧化物亲和色谱(MOAC)和固定化金属离子亲和色谱(IMAC)是目前最常用的两种磷酸肽富集方法。由于这两种方法对不同类型的磷酸肽序列具有选择性,我们提供多种柱式、吸头及试剂盒产品,以满足不同研究应用和实验目标的需求。
磷酸化肽富集试剂盒
 |  |  |  |  | |
|---|---|---|---|---|---|
| Fe-NTA磁珠法磷酸肽富集试剂盒 | Fe-NTA 磷酸肽富集试剂盒 | TiO2 磷酸肽富集与纯化试剂盒 | 石墨离心柱 | TiO2 磷酸肽富集吸头 | |
| 结合/标记机制 | 金属螯合物对磷酸基团的亲和作用 | 金属螯合物对磷酸基团的亲和作用 | 金属氧化物对磷酸基团的亲和作用 | 石墨对亲水性肽的亲和作用 | 金属氧化物对磷酸基团的亲和作用 |
| 富集策略 | Fe-NTA 磁珠 | IMAC琼脂糖树脂 | 球形多孔 TiO2 | 石墨离心柱 | 球形多孔 TiO2 |
| 上样量/反应* | 25–1,000 µg | 0.5–5 mg | 0.5–3 mg | 100 µg | 300–1,000 µg |
| 形式 | 磁珠 | 离心柱 | 吸头 | 离心柱 | 离心吸头 |
| 处理时间 | <45 分钟 | 45–60 分钟 | 45–60 分钟 | 10–20 分钟 | 35–45 分钟 |
| 立即订购 | 立即订购 | 立即订购 | 立即订购 | 立即订购 |
*每次反应的上样量基于典型哺乳动物培养细胞蛋白酶解样品计算
Thermo Scientific Pierce 激酶富集试剂盒采用 ActivX™ ATP 或 ADP 探针,对 ATP 酶(包括激酶、分子伴侣及代谢酶)活性位点进行共价标记。该类探针包含一种可与胺基反应的核苷酸类似物,以及一个 desthiobiotin(去硫生物素,生物素类似物)标签,从而实现对激酶活性位点中赖氨酸残基的选择性标记,并可进一步对已标记蛋白进行富集与回收。
这些特性使其能够用于不同样品中目标酶类别的鉴定与谱分析,或用于评估酶抑制剂的特异性和亲和力。
在质谱工作流程中,desthiobiotin 标记的蛋白首先进行还原、烷基化处理,并经酶解生成肽段。随后,仅对携带 desthiobiotin 标记的活性位点肽进行富集,并通过 LC-MS/MS 进行分析,从而实现对抑制剂全局靶点及潜在脱靶的鉴定。
激酶富集试剂盒
 | ||
|---|---|---|
| ATP 探针激酶富集试剂盒 | ADP 探针激酶富集试剂盒 | |
| 结合/标记机制 | 生物素化 ATP 类似物与活性位点赖氨酸结合 | 生物素化 ADP 类似物与活性位点赖氨酸结合 |
| 富集策略 | 固定化链霉亲和素琼脂糖树脂 | 固定化链霉亲和素琼脂糖树脂 |
| 上样量/反应* | 冻干形式(Lyophilized) | |
| 形式 | 离心柱 | 离心柱 |
| # 洗脱级分数 | 1 | 1 |
| 处理时间 | 6.5 小时 + 酶解 | 6.5 小时 + 酶解 |
| 立即订购 | 立即订购 |
其他用于质谱分析的肽段富集&分馏产品
重点数据
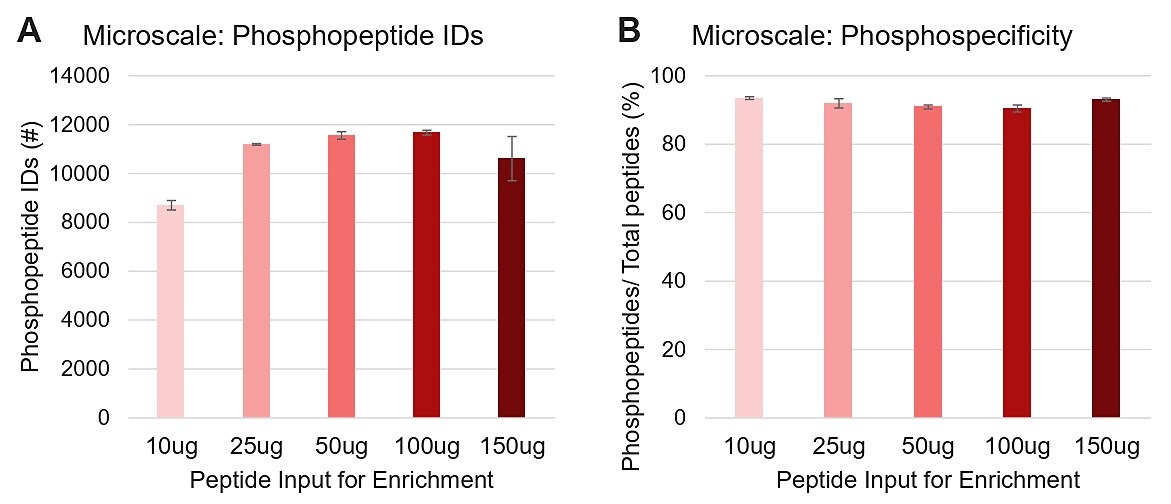
图1. High-Select 磁珠在微量尺度下的磷酸肽富集效果。在富集前,对经诺考达唑(Nocodazole)处理的 HeLa 细胞进行样品制备和定量,随后使用 High-Select Fe-NTA 磁珠进行富集。磁珠与样品的比例保持恒定(1:50,w/w),而肽样品输入量在 10–150 µg 范围内变化。结果显示,在 25–150 µg 输入量范围内,鉴定到的磷酸肽数量基本相当;当输入量为 10 µg 时,磷酸肽数量下降约 27%(A)。对于所有输入量条件,磷酸化特异性均保持在 90% 以上(B)。
每个肽段上的磷酸基团数量
| 1 | 2 | 3 | 4 | 5 | 6 | 总数 | |
|---|---|---|---|---|---|---|---|
| TiO2 | 492 | 103 | 8 | 4 | 0 | 1 | 608 |
| Fe-NTA IMAC | 234 | 34 | 216 | 3 | 1 | 0 | 488 |
| 重叠部分 | 155 | 0 | 1 | 0 | 0 | 0 | 156 |
通过TiO2与Fe-NTA IMAC对单磷酸化和多磷酸化肽段的选择性富集。基于重复实验的平均磷酸肽富集结果,展示两种方法分别富集的含 1个或多个磷酸基团 的磷酸肽数量。肽段谱图总结结果从 Proteome Software Scaffold 3.0 导出,并通过 Microsoft™ Excel™ 软件 分析。
关键结论
- TiO2:适合单磷酸化肽段的高效富集(如信号转导研究)。
- Fe-NTA IMAC:适用于多磷酸化肽段(如核酸结合蛋白或高度修饰蛋白分析)。
- 联合使用:结合两种方法可提升磷酸化蛋白质组覆盖度(减少“盲区”)。

图1. High-Select 磁珠在微量尺度下的磷酸肽富集效果。在富集前,对经诺考达唑(Nocodazole)处理的 HeLa 细胞进行样品制备和定量,随后使用 High-Select Fe-NTA 磁珠进行富集。磁珠与样品的比例保持恒定(1:50,w/w),而肽样品输入量在 10–150 µg 范围内变化。结果显示,在 25–150 µg 输入量范围内,鉴定到的磷酸肽数量基本相当;当输入量为 10 µg 时,磷酸肽数量下降约 27%(A)。对于所有输入量条件,磷酸化特异性均保持在 90% 以上(B)。
每个肽段上的磷酸基团数量
| 1 | 2 | 3 | 4 | 5 | 6 | 总数 | |
|---|---|---|---|---|---|---|---|
| TiO2 | 492 | 103 | 8 | 4 | 0 | 1 | 608 |
| Fe-NTA IMAC | 234 | 34 | 216 | 3 | 1 | 0 | 488 |
| 重叠部分 | 155 | 0 | 1 | 0 | 0 | 0 | 156 |
通过TiO2与Fe-NTA IMAC对单磷酸化和多磷酸化肽段的选择性富集。基于重复实验的平均磷酸肽富集结果,展示两种方法分别富集的含 1个或多个磷酸基团 的磷酸肽数量。肽段谱图总结结果从 Proteome Software Scaffold 3.0 导出,并通过 Microsoft™ Excel™ 软件 分析。
关键结论
- TiO2:适合单磷酸化肽段的高效富集(如信号转导研究)。
- Fe-NTA IMAC:适用于多磷酸化肽段(如核酸结合蛋白或高度修饰蛋白分析)。
- 联合使用:结合两种方法可提升磷酸化蛋白质组覆盖度(减少“盲区”)。
资源
仅供科研使用,不可用于诊断目的。