Search
总蛋白定量方法
蛋白质浓度定量是涉及蛋白质提取、纯化、标记或分析的任何实验室工作流程中不可或缺的一部分。Pierce蛋白质测定法根据测定时间、灵敏度、兼容性、标准曲线线性和蛋白间差异,提供了多种准确测定蛋白质浓度的选择。尽管本文以Pierce蛋白质测定产品为例,但所讨论的原理和化学方法普遍适用于大多数现有的比色法或荧光法蛋白质测定技术。
介绍
蛋白质定量通常是在利用色谱、电泳和免疫化学技术对蛋白样品进行分离、纯化和分析之前所必需的。根据所需的准确度以及可获得的蛋白质量和纯度,确定蛋白质浓度的方法也有所不同。
测定溶液中蛋白质浓度最简单、最直接的方法是测量其在280 nm(紫外区)的吸光度。含有芳香族侧链的氨基酸(如酪氨酸、色氨酸和苯丙氨酸)具有很强的紫外光吸收能力。蛋白质和肽的紫外吸收与其芳香族氨基酸的含量及总浓度成正比。另一种传统上用于高效液相色谱(HPLC)氨基酸分析的方法,是用有色或荧光染料(如茚三酮或邻苯二甲醛,OPA)标记所有伯胺(即N端和赖氨酸残基的侧链)。直接紫外吸收法和HPLC试剂法各有缺点,这使得这些方法在蛋白质组学工作流程中处理常规蛋白样品时并不实用。紫外吸收法不适用于蛋白混合物,因为不同蛋白质的芳香族氨基酸含量不同,吸收特性也不同。此外,任何能吸收紫外光的非蛋白成分都会干扰测量结果。
为克服这些缺点,已经开发出多种基于比色和荧光的蛋白质检测试剂方法,这些方法几乎被所有从事蛋白质研究的实验室所采用。将蛋白样品加入试剂后,会根据加入量的不同产生颜色变化或荧光增强。蛋白质浓度通过与已知浓度的纯化参考蛋白标准曲线进行对比来确定。
表1. 蛋白质测定方法的类型、优点、缺点及示例。
| 方法 | 优点 | 缺点 | 代表性检测试剂 |
|---|---|---|---|
| 紫外吸收法 |
|
| |
| 双缩脲法:蛋白质-铜螯合及还原铜的二次检测 |
|
| BCA法 Lowry法 |
| 比色染料法:蛋白质-染料结合及直接检测颜色变化 |
|
| Bradford法 |
| 荧光染料法:蛋白质-染料结合及直接检测结合染料后荧光增强 |
|
| EZQ荧光法 Qubit蛋白定量法 NanoOrange蛋白定量法 CBQCA Plus蛋白定量法 |
蛋白定量方法的选择
选择合适的蛋白定量试剂盒对于准确可靠地测定样品中的总蛋白浓度至关重要。有许多因素可能影响哪种蛋白定量方法最适合特定的实验,包括:
兼容性:确保所选的试剂盒与您的样品类型兼容,例如细胞裂解液、组织提取物、纯化蛋白或多肽。此外,还要考虑与样品中任何添加剂或去污剂的兼容性。一些常见的可能干扰蛋白定量方法的物质包括还原剂(如DTT)和去污剂(如Triton X-100)。通常,含有还原剂或铜螯合剂的样品更适合采用考马斯亮蓝染料法(Bradford法)进行分析。这是因为考马斯染料法(如Pierce Bradford和Pierce Bradford Plus试剂盒)与还原剂兼容,并且不需要铜-蛋白结合反应。对于含有去污剂的样品,铜基蛋白定量方法(如Pierce Dilution-Free Rapid Gold BCA Assay)是更好的选择,因为它们不会被低至中等量的去污剂抑制。
灵敏度:试剂盒的灵敏度决定了其检测样品中低浓度蛋白的能力。请考虑检测下限,并选择能够测量您所需范围内蛋白浓度的试剂盒。Micro BCA、NanoOrange 或 CBQCA Plus 具有极佳的灵敏度,非常适合稀释样品总蛋白浓度的定量。
线性范围:试剂盒的线性范围指的是在该范围内,蛋白定量方法能够提供准确且线性的结果。选择覆盖您样品预期浓度范围的试剂盒非常重要。当需要分析蛋白浓度变化较大的样品时,Pierce Dilution-Free Rapid Gold BCA Assay 和 Qubit Protein BR Assay 提供了最大的线性范围,非常适合起始浓度大于2 mg/mL的样品。
准确性和精密性:通过评估试剂盒的蛋白质间变异性和线性关系,来判断其准确性和精密性。应选择能够在重复实验之间产生最小变异且结果准确的试剂盒。铜螯合类检测方法,如Pierce BCA蛋白定量试剂盒,与染料结合法相比,蛋白质间的变异性更小。
使用简便性:考虑试剂盒的操作简易性、所需步骤数量、孵育时间和温度,以及需要分析的样本数量。例如,免稀释快速金色BCA蛋白定量试剂盒通过免去样品和标准品稀释步骤,将检测准备时间缩短高达80%。此外,仅需在室温下孵育5分钟。免稀释BSA蛋白标准品也可用于BCA蛋白定量试剂盒和 Bradford Plus蛋白定量试剂盒。应选择说明清晰、步骤简化、结果快速可靠的试剂盒。
分光光度计或酶标仪的可用性:不同的蛋白定量试剂盒采用不同的检测方法(比色法或荧光法)和检测格式(单管或微孔板)。在选择蛋白定量方法前,需确保有合适的仪器可用,并且仪器与检测类型和格式兼容。了解更多关于微孔板检测仪的信息。
Pierce免稀释快速金色BCA蛋白定量试剂盒和 Bradford Plus蛋白定量试剂盒相互补充,提供了适用于大多数样品的两种基本方法。这两种试剂盒的多种辅助试剂和替代版本可满足更多样品需求。
- 下载:蛋白定量方法兼容性表
- 探索:蛋白定量方法选择指南
选择蛋白标准品
由于蛋白质的氨基酸组成不同,每种蛋白质在不同类型的蛋白定量分析中反应也有所差异。因此,作为参考标准的最佳选择是使用样品中最丰富蛋白质的纯化、已知浓度的形式。但通常很难实现这一点,而且这样做往往既不方便也没有必要。在许多情况下,目标只是估算总蛋白浓度,蛋白之间的微小差异是可以接受的。
如果无法获得高度纯化的目标蛋白,或者将其作为标准品的成本过高,可以选择在所选蛋白定量方法中产生非常相似颜色反应曲线且任何实验室随时都能获得的蛋白质。通常,牛血清白蛋白(BSA)因其高纯度、广泛可得且价格相对低廉,是很好的蛋白标准品。或者,在测定抗体浓度时,牛γ球蛋白(BGG)也是一个很好的标准品,因为BGG产生的颜色反应曲线与免疫球蛋白G(IgG)非常相似。
为了最大程度地准确估算未知样品中的总蛋白浓度,每次进行蛋白定量分析时都必须包含一条标准曲线。对于那些产生非线性标准曲线的蛋白定量方法来说,这一点尤为重要。决定用于定义标准曲线的标准品数量和重复次数,取决于标准曲线的非线性程度以及所需的准确度。一般来说,如果颜色反应是线性的,构建标准曲线所需的点数会更少。通常,每个标准点至少做两个重复来构建标准曲线。
- 了解更多:蛋白定量分析数据分析
- 探索:蛋白质测定标准
蛋白质测定的样品制备
在分析样品的总蛋白含量之前,必须先将其溶解,通常是在缓冲的水溶液中进行。通常还会采取额外的预防措施,以抑制微生物生长或避免样品被外来杂质(如灰尘、毛发、皮肤或体油)随意污染。
根据蛋白质测定前所涉及的程序和样品来源,样品中会含有多种非蛋白成分。了解这些成分对于选择合适的测定方法以及评估异常结果的原因至关重要。例如,组织和细胞通常使用含有表面活性剂(洗涤剂)、生物杀灭剂(抗菌剂)和蛋白酶抑制剂的缓冲液进行裂解。还可能加入不同的盐、变性剂、还原剂和变构剂。经过过滤或离心去除细胞碎片后,典型样品中仍然会包含核酸、脂类和其他非蛋白化合物。
每种类型的蛋白定量分析都会受到某些物质的不利影响。如果蛋白溶液中的组分会人为地抑制反应、增强反应,或使背景值升高达到某个任意设定的程度(例如,与对照相比增加10%),则这些组分在蛋白定量分析中被视为干扰物质。
通过将蛋白标准品与待测蛋白在同一缓冲液中制备,可以消除少量干扰物质导致的不准确性。对于更高且不兼容的干扰物质水平,则需要采用其他策略:
- 选择不同的蛋白定量分析方法,或选择同一方法中包含克服干扰组分的版本。
- 通过透析或脱盐去除样品中分子量较小(即低于1000道尔顿)的干扰物质,如还原剂。
- 用三氯乙酸(TCA)或其他适当试剂沉淀蛋白,去除含有干扰组分的溶液,然后将蛋白重新溶解以进行分析。该示意图概述了蛋白透析方法如何用于去除可能污染蛋白样品并干扰后续应用的物质。
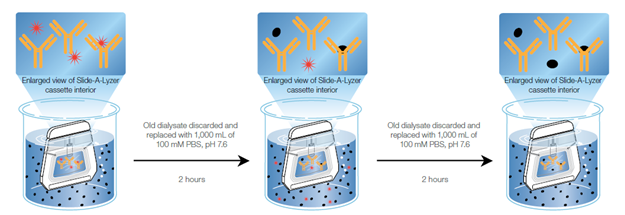
图1. 此示意图展示了如何使用透析盒进行蛋白纯化。将3毫升1毫克/毫升的IgG溶于0.1 M Tris缓冲液(pH 7),放入透析盒中,再将透析盒置于1000毫升100 mM PBS缓冲液(pH 7.6)中。弃去旧的透析液,换入1000毫升100 mM PBS缓冲液(pH 7.6)。IgG分子太大,无法进入膜上的孔,因此透析盒内的IgG量保持不变。随着Tris缓冲液向外扩散、PBS缓冲液向内扩散,透析盒内Tris缓冲液浓度降至低于0.01 M。再次弃去旧的透析液,换入1000毫升100 mM PBS缓冲液(pH 7.6)。透析盒内的IgG仍保持不变。透析盒内的Tris缓冲液降至几乎不可检测的水平。透析盒内的缓冲液为100 mM PBS,pH 7.6。
- 下载:消除干扰物质
蛋白质间的变异性
在特定的蛋白质测定中,样品中的每种蛋白质都会产生独特的响应。这种蛋白质间的变异性是指在使用相同方法同时检测相同质量的不同蛋白质时,所获得的颜色(吸光度)量的差异。这些颜色响应的差异与氨基酸序列、等电点(pI)、二级结构以及某些侧链或辅基的存在有关。
根据样品类型和进行测定的目的,蛋白质间的变异性是选择蛋白质测定方法以及合适的测定标准(如BSA与BGG)时需要考虑的重要因素。基于相似化学原理的蛋白质测定方法,其蛋白质间的变异性也相似。

图2. 标准曲线。使用Pierce BCA蛋白质测定试剂盒对纯化的BSA和BGG进行标准曲线绘制,展示了两种不同蛋白质产生的颜色强度差异。
蛋白质测定方法在检测蛋白质特异性官能团的化学基础上各不相同。有些测定方法能够检测肽键,但没有任何一种方法能专一地只检测肽键。实际上,每种蛋白质测定方法对一种或几种特定氨基酸的灵敏度高于其他氨基酸。因此,在任何一种蛋白质测定中,不同氨基酸组成的蛋白质会以不同的速率或强度产生颜色。
下表比较了几种Thermo Scientific Pierce蛋白质测定方法在颜色响应上的蛋白质间变异性。这些数据可作为评估不同蛋白质样品响应差异的一般参考。然而,由于这些比较是在相同蛋白质浓度和缓冲液条件下进行的,因此不应将其作为精确的校准因子使用。
这些变异性信息有助于选择合适的蛋白质标准。例如,当待测样品为纯化抗体时,牛γ球蛋白(BGG,蛋白质#2)作为标准会比牛血清白蛋白(BSA,蛋白质#1)更准确。这些数据还表明,在报告蛋白质测定结果时,明确所用的测定标准非常重要。
对于这里展示的每种蛋白质测定方法,使用标准试管协议对10种蛋白质进行了测定。计算了每种蛋白质的净(空白校正后)平均吸光度。每种蛋白质的净吸光度以与BSA的净吸光度的比值表示(例如,0.80的比值表示该蛋白质产生的颜色为等质量BSA的80%)。所有蛋白质的浓度均为1000 µg/mL。
表2. 蛋白质测定方法概览。
| 结果 | 免稀释快速金色BCA | 标准BCA | 还原型BCA | 微量BCA | 考马斯 | 考马斯Plus | 660 nm |
| 变异系数(%) | 20.67 | 20.52 | 22.03 | 17.78 | 41.57 | 37.62 | 22.70 |
| 标准差 | 0.23 | 0.20 | 0.22 | 0.20 | 0.29 | 0.28 | 0.17 |
| 平均比值 | 1.10 | 0.97 | 1.01 | 1.11 | 0.69 | 0.75 | 0.74 |
| 检测的蛋白质 | |||||||
| 1. 牛血清白蛋白 | 1.00 | 1.00 | 1.00 | 1.00 | 1.00 | 1.00 | 1.00 |
| 2. 牛伽马球蛋白 | 1.32 | 1.29 | 1.36 | 1.33 | 0.62 | 0.67 | 0.53 |
| 3. 转铁蛋白 | 1.17 | 0.93 | 0.97 | 1.09 | 0.93 | 0.96 | 0.79 |
| 4. 溶菌酶 | 1.28 | 1.25 | 1.38 | 1.51 | 0.53 | 0.68 | 0.78 |
| 5. β-乳球蛋白 | 0.97 | 0.85 | 0.74 | 0.85 | 0.29 | 0.33 | 0.66 |
| 6. 卵白蛋白 | 1.01 | 1.00 | 1.01 | 1.09 | 0.49 | 0.78 | 0.62 |
| 7. 蛋白A | 0.57 | 0.60 | 0.70 | 0.89 | 0.28 | 0.22 | 0.75 |
| 8. 己糖激酶 | 1.14 | 0.99 | 0.97 | 1.11 | 0.87 | 0.87 | 0.50 |
| 9. 纤维蛋白原 | 1.33 | 1.01 | 1.11 | 1.17 | 0.86 | 0.96 | 0.81 |
| 10. 碳酸酐酶 | 1.21 | 0.82 | 0.90 | 1.04 | 1.05 | 1.06 | 0.97 |
计算与数据分析
在大多数蛋白质测定中,样品蛋白质浓度是通过将其测定反应与一系列已知浓度的标准品的反应进行比较来确定的。蛋白质样品和标准品以相同方式处理,即与测定试剂混合后,使用分光光度计测量吸光度。标准品的反应结果用于绘制或计算标准曲线。未知样品的吸光度值随后被插入到标准曲线的图表或公式中,以确定其浓度。
显然,只有在未知样品和标准品被完全相同地处理时,才能获得最准确的结果。这包括尽可能在相同时间和相同缓冲液条件下进行测定。由于涉及不同的移液步骤,如果需要计算统计数据(如标准差、变异系数)以考虑随机误差,则有必要进行重复实验。

图3. 点对点法与线性拟合法标准曲线的比较。对于吸光度为0.6的测试样品进行插值和计算时,所得蛋白质浓度值有显著差异。在这种情况下,点对点法显然为测试样品的计算提供了更准确的参考线。
尽管大多数现代分光光度计和酶标仪都配备了用于蛋白质测定数据分析的内置软件程序,但技术人员常常对其中的几个因素存在误解。花几分钟学习并正确应用这些计算原理,可以极大提升设计实验的能力,从而获得尽可能准确的结果(参见相关技术提示和链接)。
- 下载:确定用于蛋白质测定的测量波长
- 下载:如何使用标准曲线
肽定量测定
对于利用质谱进行蛋白质组学的工作流程,在蛋白质消化、富集和/或C18纯化步骤后测量肽浓度非常重要,以便规范化样本之间的差异。特别是在使用等标记实验时,必须确保在混合前对等量样品进行标记,以获得准确的结果。
与蛋白质测定方法类似,有多种方法可用于测定肽浓度。传统上,紫外-可见光(A280)或比色法、试剂法蛋白质测定技术被用于测量肽浓度。BCA和微量BCA测定常被使用。虽然这些方法对蛋白样品效果良好,但这些试剂并不适用于准确检测肽。作为替代,专门用于肽混合物定量的肽定量测定(比色法或荧光法格式)也可选用。在决定使用比色法或荧光法微孔板测定格式进行肽定量时,必须考虑以下重要标准:
- 与样品类型、组分和工作流程的兼容性
- 测定范围和所需样品体积
- 检测样本数量时的速度和便利性
- 测定分析结果所需的分光光度计或荧光光度计的可用性
这些代表性数据比较了使用比色法和荧光法分析获得的结果。

图4. 比色法与荧光法肽分析的定量比较。十二种细胞系制备了胰蛋白酶肽消化液。根据说明书,使用 Thermo Scientific Pierce定量比色肽分析试剂盒和 Pierce定量荧光肽分析试剂盒测定肽消化液浓度。每个样品均做三次重复实验,并用蛋白消化液分析标准品生成的标准曲线计算每个消化液的浓度。
推荐阅读
- Bradford, MM. (1976) 利用蛋白质-染料结合原理对微克级蛋白质进行定量的快速灵敏方法。《分析生物化学》,72, 248-254。
- Smith, P.K, Krohn R.I., Hermanson G.T., 等. (1987) 使用双辛可宁酸测定蛋白质。《分析生物化学》,150, 76-85。
- Krohn, R.I.(2002)。蛋白质总量的比色检测与定量,《细胞生物学当前实验方案》,A.3H.1-A.3H.28,约翰威立父子公司。
- Krohn, R.I.(2001)。蛋白质总量的比色测定,《食品分析化学当前实验方案》,B1.1.1-B1.1.27,约翰威立父子公司。
- Lowry, O.H., Rosebrough, N.J., Farr, A.L. 等(1951)使用福林酚试剂测定蛋白质含量。《生物化学杂志》,193, 265-75。
- Legler G, Müller-Platz CM, Mentges-Hettkamp M 等(1985)Lowry蛋白质测定的化学基础。《分析生物化学》,150, 278-87。
相关文献
- 技术提示:消光系数与蛋白质浓度
仅供科研使用,不可用于诊断目的。